2-3-2外界因素对化学反应速率的影响【学习目标】1
理解浓度、压强、催化剂对化学反应速率的影响
知道反应速率常数、活化能的含义,能够根据相应规律解决有关问题
【学习重难点】学习重点:浓度、压强、催化剂对化学反应速率的影响
学习难点:浓度、压强、催化剂对化学反应速率的影响
【自主预习】1.根据课本试自学有关碰撞理论的知识
(1)有效碰撞:能够引发的碰撞
(2)活化分子:能够发生的分子
(3)活化能:活化分子比普通分子所多出的那部分能量
活化能越小,普通分子就越变成活化分子
如图所示:反应的活化能是,反应热是
(4)普通分子+活化能活化分子
(5)活化能与化学反应速率的关系:在一定条件下,活化分子所占的百分数是的
活化分子的越大,单位体积内越多,单位时间内的次数越多,化学反应速率
活化能降低→普通分子变成活化分子→活化分子百分数增大→有效碰撞次数增多→反应速率加快
2.影响化学反应速率的主要因素是的性质,不同化学反应具有的反应速率
外界条件对化学反应速率也产生影响
【预习检测】1.决定化学反应速率的内因是()①温度②压强③催化剂④浓度⑤反应物本身的性质A.①②③④⑤B.⑤C.①④D.①②③④2.对于反应:2SO2+O22SO3,当其他条件不变时,只改变一个反应条件,将生成SO3的反应速率的变化填入下表空格里(填“增大”、“减小”或“不变”)
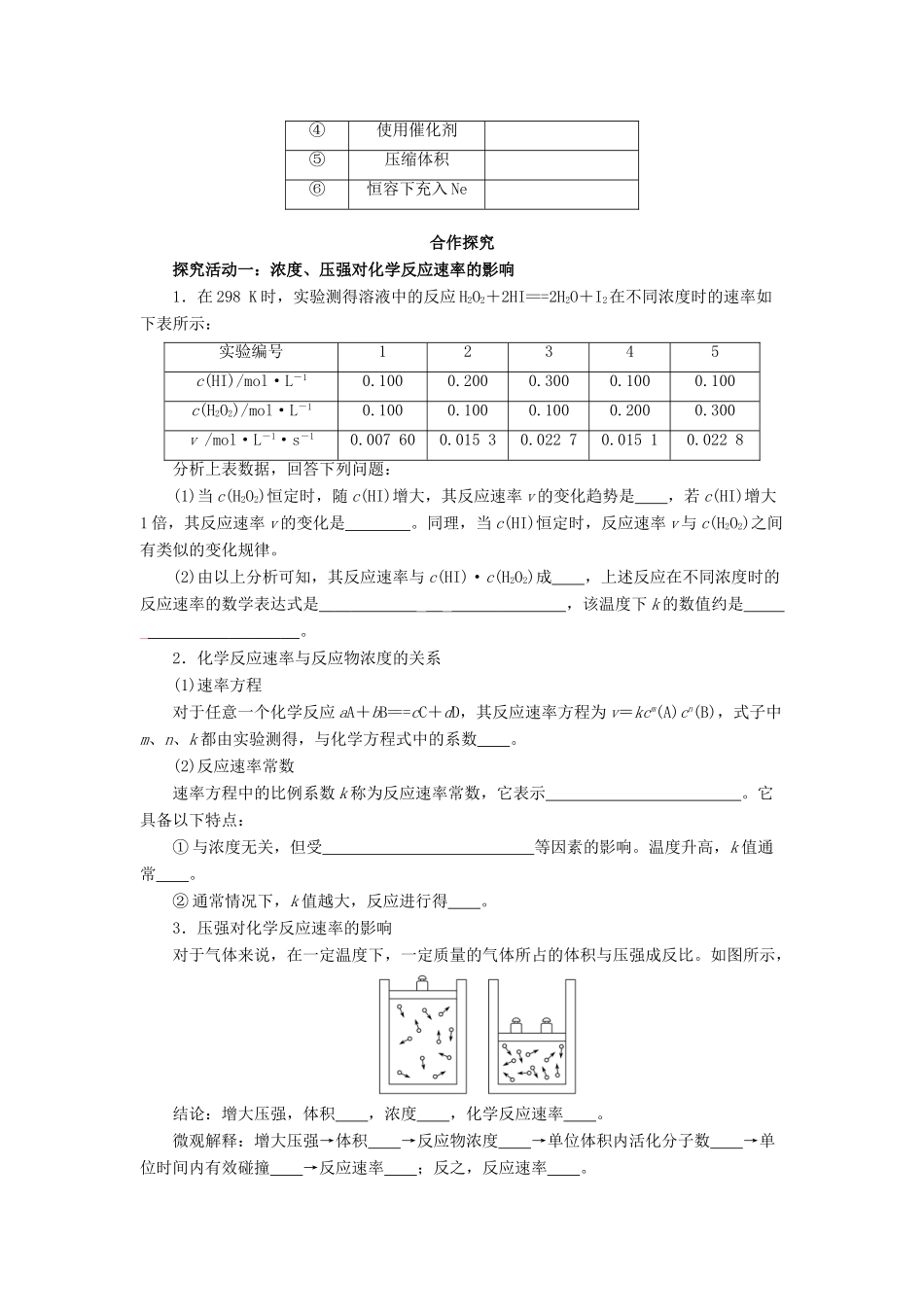
编号改变的条件生成SO3的速率①升高温度②降低温度③增大O2的浓度④使用催化剂⑤压缩体积⑥恒容下充入Ne合作探究探究活动一:浓度、压强对化学反应速率的影响1.在298K时,实验测得溶液中的反应H2O2+2HI===2H2O+I2在不同浓度时的速率如下表所示:实验编号12345c(HI)/mol·L-10
100c(H2O2)/mol·L-10