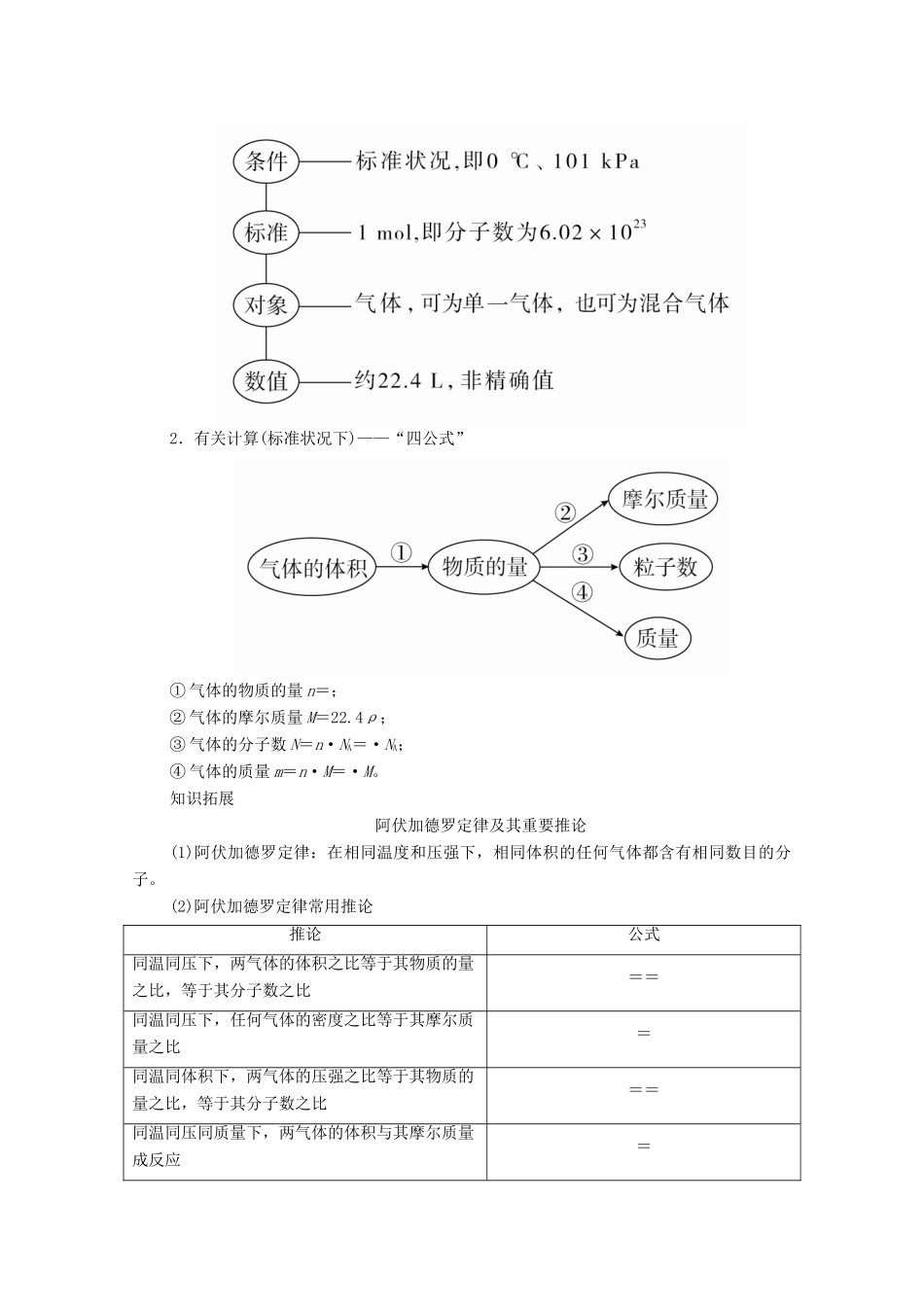
第3课时物质的聚集状态[学习目标]1.了解气体摩尔体积的含义。2.掌握标准状况下有关气体摩尔体积的计算。一、物质的聚集状态1.晶体固体可分为两类,一类为□晶体,另一类为□非晶态物质。构成晶体的微粒在空间的排列是有规则的,因此在通常情况下,晶体具有规则的几何外形,具有固定的熔点。构成非晶态物质的微粒在空间的排列没有规则,因此非晶态物质没有固定的熔点,一般不具有规则的几何外形。常见的氯化钠、纯碱、冰和各种金属都属于晶体,而玻璃属于非晶态物质。2.物质的聚集状态主要有□气态、液态和固态三种。同一物质在不同的温度和压强下,其聚集状态可能不同。不同物质在同一温度及压强下,其聚集状态也可能不同。不同聚集状态物质的特性:3.影响物质体积大小的因素(1)在温度和压强一定时,物质的体积决定于三个因素:□微粒的数目、微粒的大小及微粒间的距离。(2)对于固体和液体来说,微粒间距离很小,在微粒数目相同的条件下,固、液态物质的体积主要决定于□微粒的大小。(3)对于气体来说,其体积大小主要取决于□气态物质中微粒之间的距离(气体分子本身大小忽略不计)和□微粒数目的多少,而微粒之间的距离取决于□外界条件(温度、压强)的影响。二、气体摩尔体积1.定义:□单位物质的量的气体所占的体积,叫气体摩尔体积,其符号是□Vm,单位是□L·mol-1或m3·mol-1。2.决定气体摩尔体积大小的因素是□气体分子间的距离;影响因素是□温度、压强。3.标准状况是指□0_℃、101_kPa时的状况,标准状况下1mol任何气体所占的体积都约是22.4L。即标准状况下的气体摩尔体积约为22.4□L·mol-1。4.气体的体积(V)、气体摩尔体积(Vm)与物质的量(n)的关系:□V=n·Vm。5.气体摩尔体积(Vm)不仅适用于纯净的气体,还适用于混合气体。例:在相同条件(温度和压强)1molO2与1mol氧气和氢气的混合气体的体积相等。理解此概念必须注意五个要点:a.必须是气体物质,不适合固体、液体;b.物质的量为1mol;c.必须是标准状况;d.体积约是22.4L;e.1mol气体所占的体积约为22.4L,但外界条件不一定是标准状况下。1.一定质量的某种气体,其体积的大小受何条件影响?提示:温度和压强,温度越高、压强越小,体积就越大。2.1molH2和1molO2的气体体积一定相同吗?提示:不一定,因为气体的体积受温度和压强的影响。3.标准状况下,1mol水的体积约为22.4L吗?提示:不是,标准状况下,水不是气体。4.气体在非标准状况下的气体摩尔体积,一定不是22.4L/mol吗?提示:不一定,气体在标准状况下的气体摩尔体积是22.4L/mol,升高温度,体积增大,增大压强,体积减小,所以,在非标准状况下,当温度和压强适当时,气体摩尔体积也可能为22.4L/mol。1.气体摩尔体积的正确理解2.有关计算(标准状况下)——“四公式”①气体的物质的量n=;②气体的摩尔质量M=22.4ρ;③气体的分子数N=n·NA=·NA;④气体的质量m=n·M=·M。知识拓展阿伏加德罗定律及其重要推论(1)阿伏加德罗定律:在相同温度和压强下,相同体积的任何气体都含有相同数目的分子。(2)阿伏加德罗定律常用推论推论公式同温同压下,两气体的体积之比等于其物质的量之比,等于其分子数之比==同温同压下,任何气体的密度之比等于其摩尔质量之比=同温同体积下,两气体的压强之比等于其物质的量之比,等于其分子数之比==同温同压同质量下,两气体的体积与其摩尔质量成反应=特别提醒:该定律及推论是非标准状况下有关气体的常用计算方法的理论依据。[练习与实践]1.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是()A.甲的分子数比乙的分子数多B.甲的物质的量比乙的物质的量少C.甲的摩尔体积比乙的摩尔体积小D.甲的相对分子质量比乙的相对分子质量小答案B解析同温同压下甲的密度大于乙的密度,说明甲的相对分子质量大,故D项错误;在等质量的前提下,甲的物质的量少,故B项正确;由于分子数与物质的量成正比,故A项错误;在同温同压下,任何气体的摩尔体积均相等,故C项错误。2.在三个体积相同的密闭容器中分别充入Ne、H2、O2三种气...