第二章电解质溶液学案电离度目的要求:掌握电离度的概念;学会有关电离度的简单计算;培养学生论述外界条件对电离度的影响能力
重点难点:电离度的概念;电离度的计算
教学方法:讲授法教学过程:引入(1)醋酸、氨水、水等是弱电解质,怎样用定量的方法来描述他们的电离程度相对大小
(2)弱酸(如:HCOOH、CH3COOHetc
)的酸性如何对比
板书一.电离度表示弱电解质在水溶液中电离程度的相对大小
当弱电解质在水溶液里达到电离平衡时,溶液中已经电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的百分数
计算公式:α=2
只适用于处于电离平衡状态的弱电解质
意义:(1)原有分子总数=已电离分子数+未电离的分子数例如:在醋酸溶液中,α=若α=1
32%,表示每10000个醋酸分子中有132个发生电离
(2)表示式可用物质的量或物质的量浓度来表示
问题在25C,求纯水的电离度
(已知:c(H+)=c(OH-)=1mol/L(3)依据电离度可以判断弱酸的酸性和盐的酸碱性(参阅表2-1,在同一条件下)弱酸:α值越大,酸性越强α值越小,酸性越弱(4)电离度的适用条件:一定温度、浓度、电离平衡时
对比不同弱电解质的电离度,只有条件相同时才有意义
板书二.影响电离度的因素:1
外因:(1)温度:因为电离过程是吸热的,因此温度升高,电离平衡向电离的方向移动,电离度增大
(2)浓度:(冰醋酸稀释对导电性的影响)现象:开始稀释时,导电性逐渐增强;到一定程度后,导电性逐渐减弱
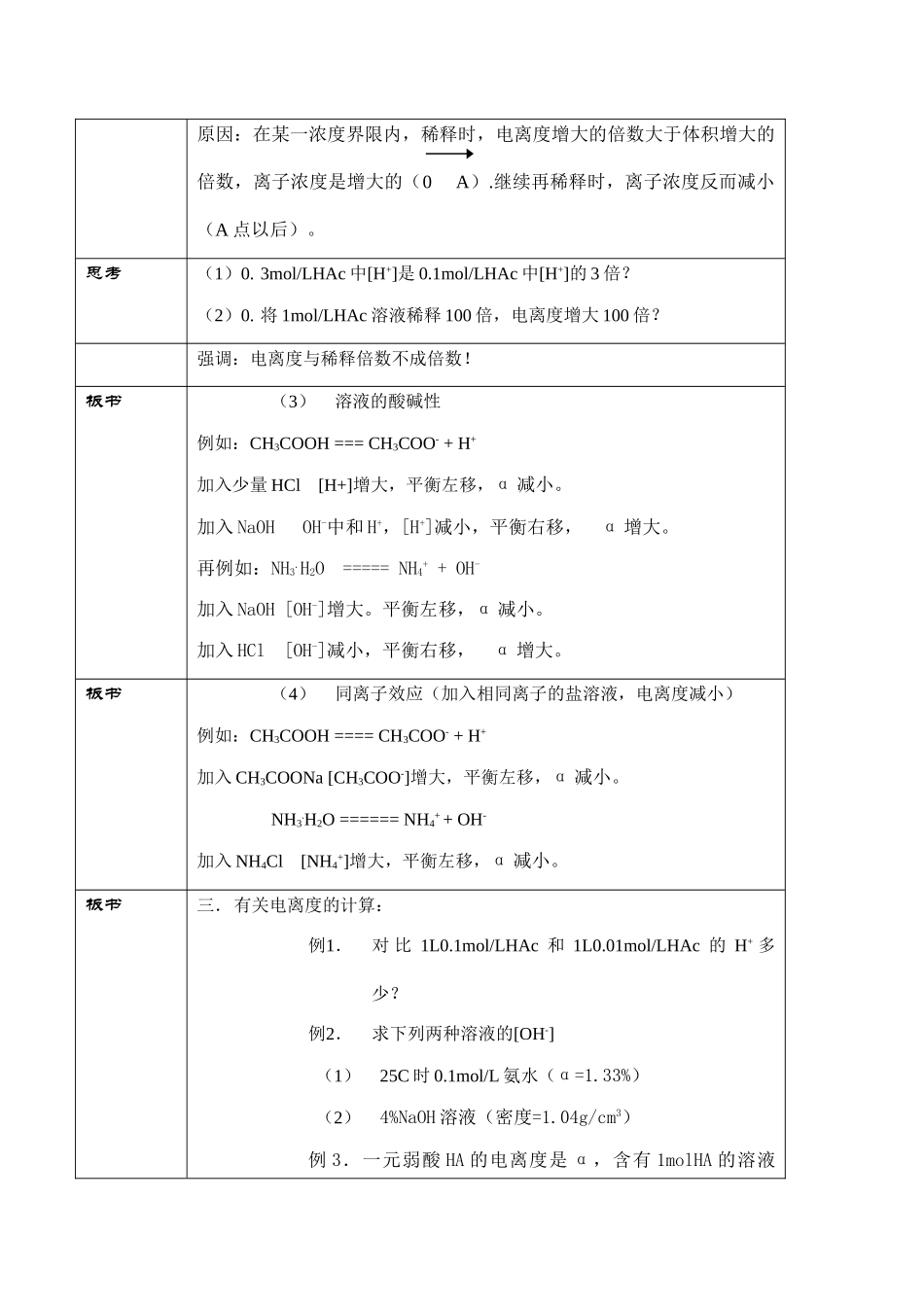
4结论:溶液浓度减小时,电离度增大,但导电性不一定增强
导电性强弱与溶液中自由移动离子浓度成正比
[H+]α0A加水量0C(mol/L)原因:在某一浓度界限内,稀释时,电离度增大的倍数大于体积增大的倍数,离子浓度是