高一化学新授课第二章第一节化学能与热能(1)一、自主学习的目标与任务:复习化学反应的实质,能从化学键的角度理解化学反应中能量变化的主要原因二、结合学习内容思考:(1)化学反应的实质是什么
(2)从微观角度怎样判断一个化学反应是吸收能量还是放出能量
(3)一个确定的化学反应是吸收能量还是放出能量是由什么决定的
三、自主解答下列各题:1
化学键的是物质在化学反应中发生能量变化的主要原因
化学反应的实质是旧的化学键和新的化学键
一个确定的化学反应是吸收能量还是放出能量,取决于反应物的总能量产物的总能量,是放热反应;反应物的总能量产物的总能量,是吸热反应
【学习目标】1、能从化学键的角度理解化学反应中能量变化的主要原因2、通过化学能与热能的相互转变,理解“能量守恒定律”【重点及难点】从本质上理解化学反应中能量的变化,从而建立起科学的能量变化观
【学习内容】一、课前自主学习检查:自查自纠二、构建知识框架、剖析典型概念(学生总结,教师点拨)课前自主学习(学案)课堂主体参与(教案)一、化学键与化学反应的能量关系以H2与Cl2的反应为例,分析反应中化学键的变化,说明此反应的实质
思考交流一:阅读课本p32内容,试从微观本质上阐述化学反应中的能量变化
思考交流二:阅读课本p32-33内容,试从宏观的角度来阐述化学反应中的能量变化
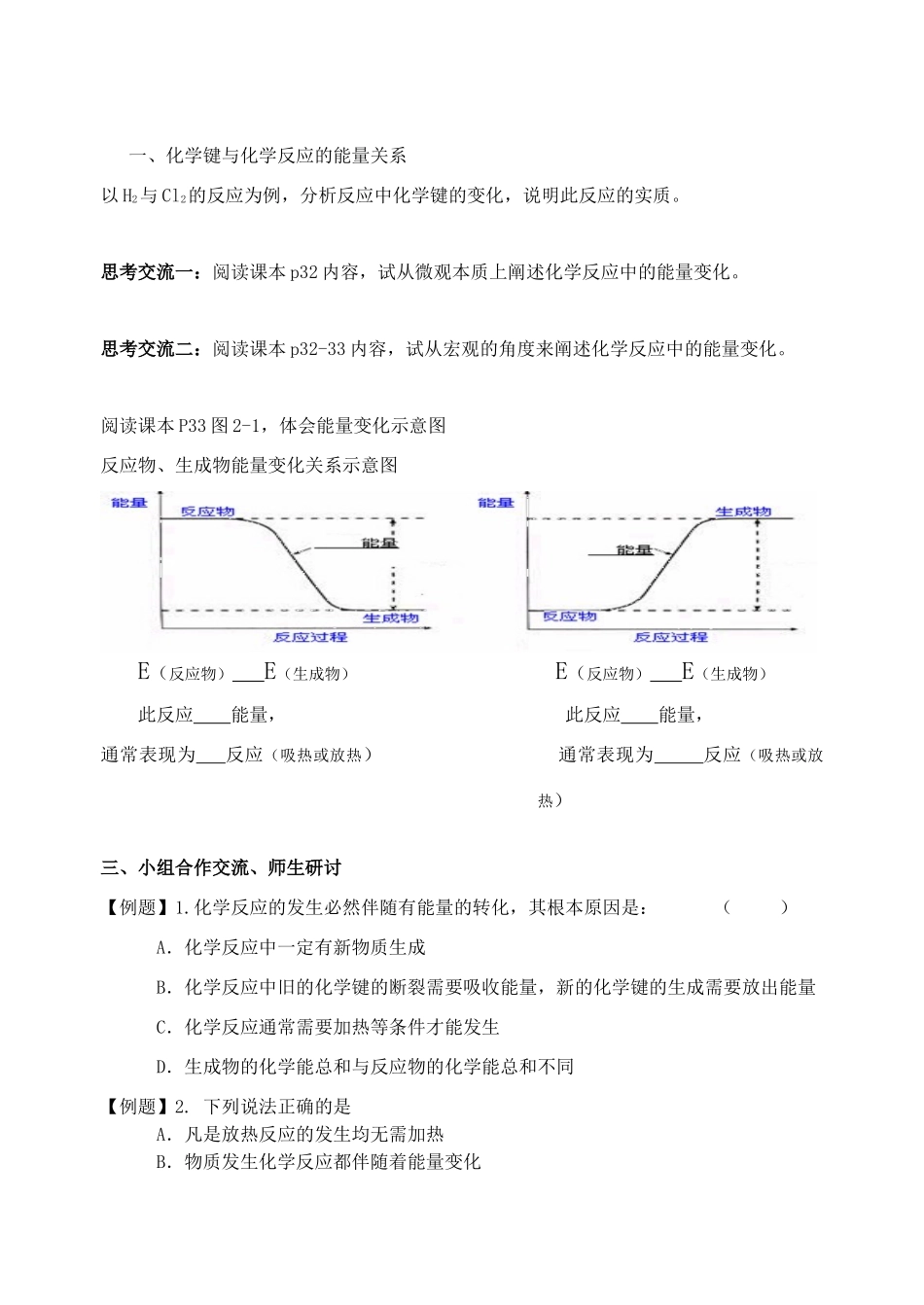
阅读课本P33图2-1,体会能量变化示意图反应物、生成物能量变化关系示意图E(反应物)E(生成物)E(反应物)E(生成物)此反应能量,此反应能量,通常表现为反应(吸热或放热)通常表现为反应(吸热或放热)三、小组合作交流、师生研讨【例题】1
化学反应的发生必然伴随有能量的转化,其根本原因是:()A.化学反应中一定有新物质生成B.化学反应中旧的化学键的断裂需要吸收能量,新的化学键的生成需要放出能量C.化学反应通常需要加热等条件才能发生D.生成物的化学能总和与反应物的