第2课时影响化学平衡移动的因素(一)浓度、压强对化学平衡移动的影响[学习目标定位]1
通过外界条件对可逆反应速率的影响,掌握化学平衡移动的内在因素
通过实验探究,讨论分析浓度、压强影响平衡移动的规律
一化学平衡状态的移动1
在一定条件下,把1molN2和3molH2充入一密闭容器中发生反应N2+3H22NH3,一段时间后达到平衡
在某一时刻,保持容器容积不变,充入N2,此时,c(N2)增大,v正增大,c(NH3)不变,v逆不变,随着反应的进行,c(N2)减小,v正减小,c(NH3)增大,v逆增大最终v正=v逆
在一定条件下,可逆反应达到化学平衡状态,如果改变影响平衡的条件(如浓度、气体反应的压强、温度等),化学平衡状态被破坏(正、逆反应速率不再相等),直至正、逆反应速率再次相等,在新的条件下达到新的化学平衡状态
这种现象称作平衡状态的移动,简称平衡移动
化学平衡移动可表示为归纳总结化学平衡移动方向的判断条件改变1
试根据下列图像判断化学平衡移动的方向
答案①向正反应方向移动;②向逆反应方向移动;③平衡不移动
二浓度对化学平衡移动的影响1
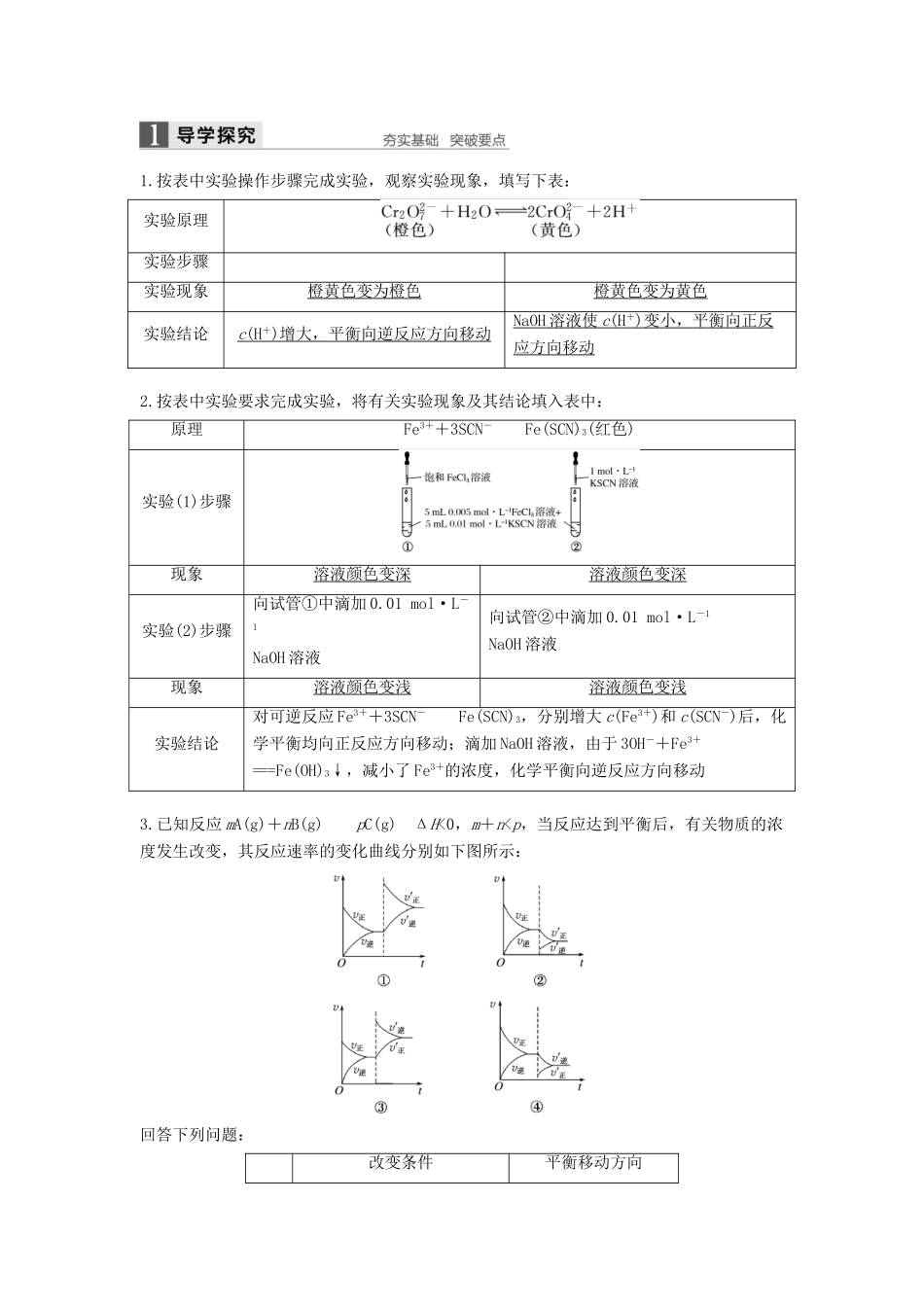
按表中实验操作步骤完成实验,观察实验现象,填写下表:实验原理实验步骤实验现象橙黄色变为橙色橙黄色变为黄色实验结论c(H+)增大,平衡向逆反应方向移动NaOH溶液使c(H+)变小,平衡向正反应方向移动2
按表中实验要求完成实验,将有关实验现象及其结论填入表中:原理Fe3++3SCN-Fe(SCN)3(红色)实验(1)步骤现象溶液颜色变深溶液颜色变深实验(2)步骤向试管①中滴加0
01mol·L-1NaOH溶液向试管②中滴加0
01mol·L-1NaOH溶液现象溶液颜色变浅溶液颜色变浅实验结论对可逆反应Fe3++3SCN-Fe(SCN)3,分别增大c(Fe3+)和c(SCN-)后,化学平衡均向正反应方向移动;滴加NaOH