实验13同周期元素金属性的递变钠、镁、铝与水、酸的反应1、掌握钠、镁、铝与水反应的原理、现象2、探究不同金属与水反应的快慢3、探究第三周期元素金属性强弱的递变规律2Na+H2O===2NaOH+H2↑Mg+2H2O===Mg(OH)2+H2↑2Na+2HCl===2NaCl+H2↑Mg+2HCl===MgCl2+H2↑2Al+6HCl===2AlCl3+3H2↑小试管、砂纸、酒精灯、镁带、铝片、1mol·L1−盐酸、水通过前面学习我们知道钠在冷水中剧烈反应,金属钠浮在水面上、熔成闪亮的小球、四处游动、发出嘶嘶的响声、溶液变红(加酚酞)
钠与盐酸反应具有钠与水反应的所有现象,但是更为剧烈
实验操作取一小段镁带和一小片铝,用砂纸除去表面的氧化膜,分别放入两支试管中
向试管中加入2ml水,并滴入2滴酚酞溶液,观察现象
过一会加热试管至水沸腾,观察现象
取一小段镁带和一小片铝,用砂纸除去表面的氧化膜,分别放入两支试管,再加入2ml1mol·L1−盐酸
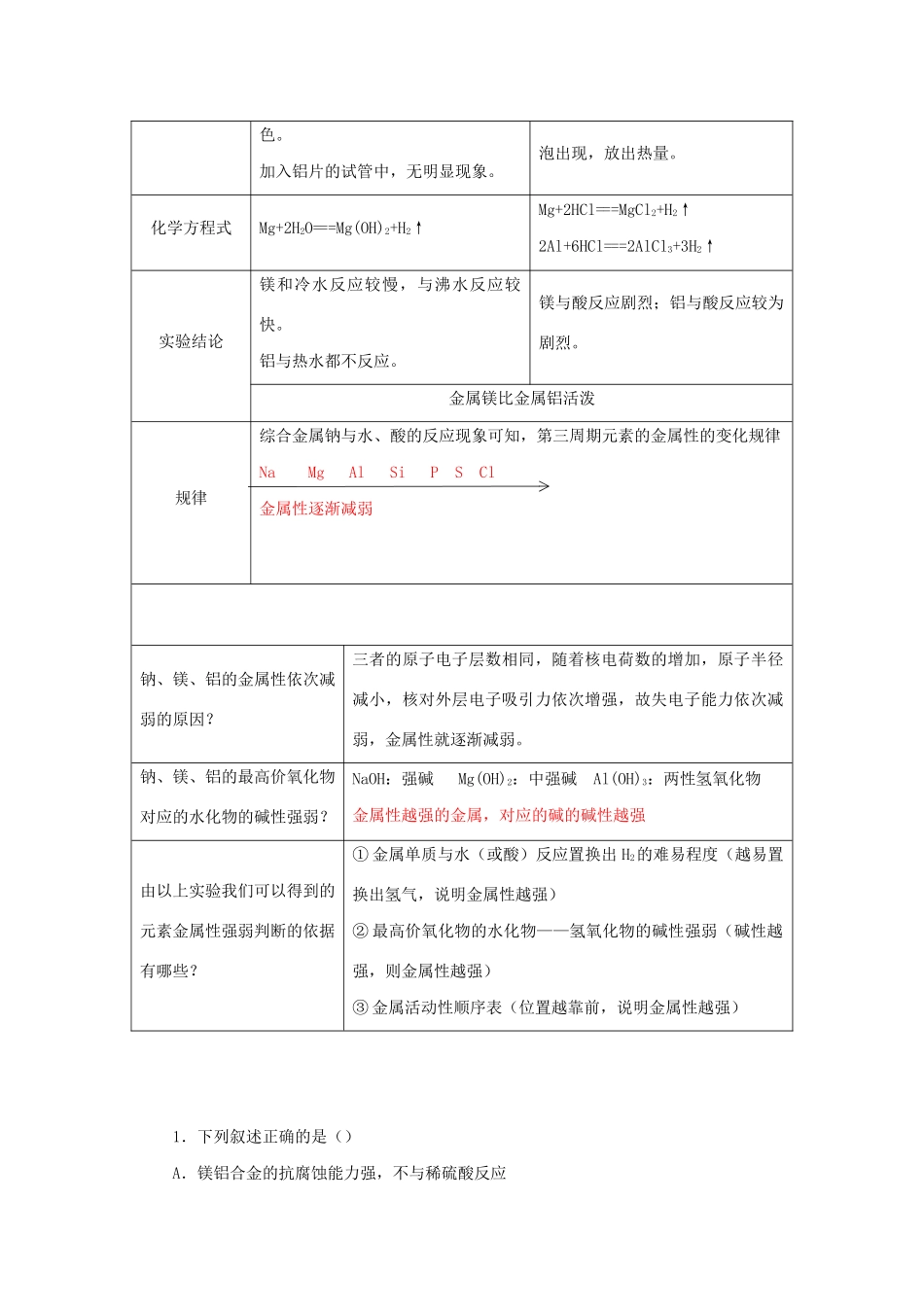
实验现象加入镁带的试管中未加热时无现象,加热后镁带上产生气泡,溶液变红镁带剧烈反应,有大量气泡出现,放出热量;铝片较迅速反应,有气色
加入铝片的试管中,无明显现象
泡出现,放出热量
化学方程式Mg+2H2O===Mg(OH)2+H2↑Mg+2HCl===MgCl2+H2↑2Al+6HCl===2AlCl3+3H2↑实验结论镁和冷水反应较慢,与沸水反应较快
铝与热水都不反应
镁与酸反应剧烈;铝与酸反应较为剧烈
金属镁比金属铝活泼规律综合金属钠与水、酸的反应现象可知,第三周期元素的金属性的变化规律NaMgAlSiPSCl金属性逐渐减弱钠、镁、铝的金属性依次减弱的原因
三者的原子电子层数相同,随着核电荷数的增加,原子半径减小,核对外层电子吸引力依次增强,故失电子能力依次减弱,金属性就逐渐减弱
钠、镁、铝的最高价氧化物对应的水化