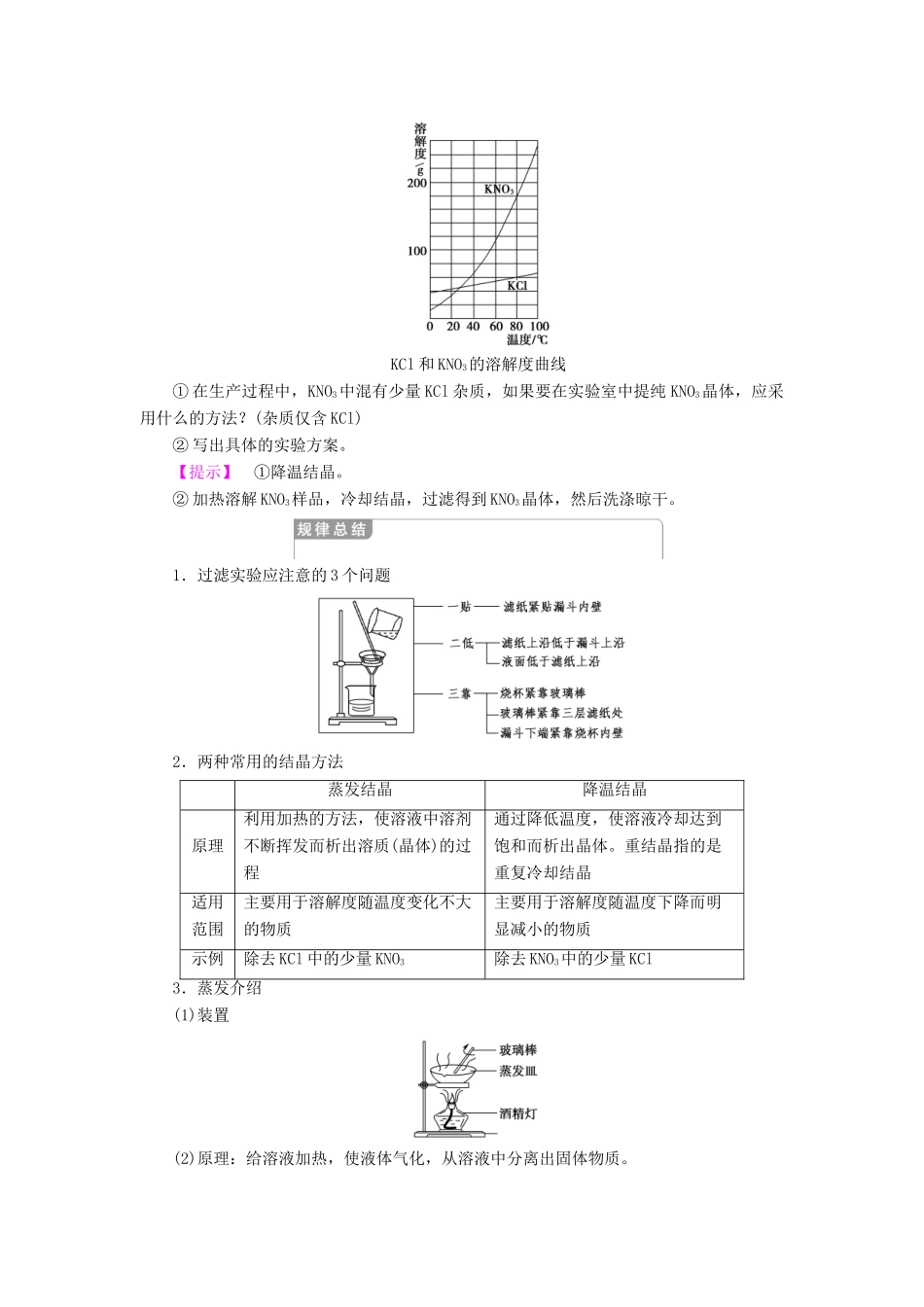
第1课时物质的分离与提纯学习目标:1.初步学会过滤、结晶、萃取和分液、蒸馏等分离物质的实验技能,能独立完成一些简单的物质分离与提纯的实验操作。(重点)2.初步了解根据物质的不同性质,来选择不同的分离方法对物质进行分离。(重难点)[自主预习·探新知]1.过滤若两种物质的混合物中,一种组分可溶于水,而另一种组分难溶于水,可以先加适量的水溶解混合物,然后过滤,将滤液蒸发结晶得到可溶解的组分,从而实现可溶性组分与难溶性组分的分离。如图过滤装置2.结晶若固体混合物中的两种组分都可溶于水,且溶解度随温度变化有较大差异,则可以参照两种物质的溶解度曲线,利用溶解、结晶的方法分离。如在提纯混有少量氯化钾的硝酸钾时,先在较高温度下将混合物溶于水中形成浓溶液,然后冷却到一定温度,由于硝酸钾的溶解度随温度降低急剧下降,因此有大量硝酸钾晶体析出,而氯化钾的溶解度随温度变化不大,因而不会结晶析出。再过滤,即可得到纯净的硝酸钾晶体。3.萃取、分液(1)利用物质在互不相溶的溶剂中溶解度的不同,将物质从一种溶剂转移到另一种溶剂中,从而实现分离的方法称为萃取。(2)萃取时,在液态混合物中加入的溶剂称为萃取剂。萃取之后,一般还要使用分液的方法将互不相溶的液体分离。在实验室中,萃取和分液通常在分液漏斗中进行。(3)当分液漏斗中的液体分成清晰的两层后,打开旋塞,将下层液体放出,然后关闭旋塞,将上层液体从上口倒出。如图装置。4.蒸馏(1)原理:利用互溶液体混合物中各组分的沸点相差较大,将其加热至某一组分的沸点,使之汽化,然后将蒸气重新冷凝为液体的操作过程。(2)仪器装置(3)应用①分离沸点相差较大的液体混合物。②除去液体中难挥发或不挥发物质。(4)注意事项①加热时为了防止液体暴沸可加入沸石或碎瓷片。②温度计水银球应插至蒸馏烧瓶的支管口处。③冷却水的流向应从冷凝管的下口进,上口出。5.粗盐的提纯除去粗盐中的杂质氯化镁及泥沙,可以先将粗盐溶于适量水中,再向粗盐水中加入稍过量的氢氧化钠溶液,使氯化镁完全转化为氢氧化镁沉淀,化学方程式为MgCl2+2NaOH===Mg(OH)2↓+2NaCl。过滤,除去泥沙和氢氧化镁沉淀,向滤液中加入盐酸中和过量的氢氧化钠,最后加热蒸发溶液,获得氯化钠晶体。[基础自测]1.判断正误(正确的打“√”,错误的打“×”)(1)为加快过滤,可用玻璃棒搅动漏斗中的溶液。()(2)蒸发结晶时最后可以将水直接蒸干再停止加热。()(3)萃取分液一般在分液漏斗中进行。()(4)用酒精作萃取剂萃取溴水中的溴。()(5)分液漏斗在使用之前必须检查是否漏水。()(6)蒸馏时可将温度计水银球插入液体中。()(7)油水混合物可用分液法分离。()【答案】(1)×(2)×(3)√(4)×(5)√(6)×(7)√2.可用于分离或提纯物质的方法有:①过滤,②蒸馏,③加热升华,④分液,⑤萃取,⑥结晶;(在下列横线上填写分离提纯的合理方法的序号)。(1)除去石灰水中悬浮的CaCO3颗粒:________。(2)除去NaCl晶体中混有的碘单质:________。(3)分离汽油和煤油的混合物:________。(4)分离水和苯的混合物:________(苯是不溶于水的液体)。(5)用四氯化碳提取溴水中的溴单质:________。(6)从含有少量氯化钠的硝酸钾溶液中提取硝酸钾:________。【答案】(1)①(2)③(3)②(4)④(5)⑤④(6)⑥[合作探究·攻重难]固—液分离的方法[思考交流](1)实验室中用KClO3在MnO2催化下受热分解制取氧气,从反应后的混合物中分离、回收KCl和MnO2,需要使用哪些分离方法?请简述实验方案。【提示】使用分离方法为过滤及蒸发结晶。实验方案:加水溶解、过滤、洗涤滤渣,即得到MnO2,将滤液蒸发结晶,可得到KCl晶体。(2)现有混有少量KCl的KNO3粉末,参照如图的溶解度曲线,回答下列问题:KCl和KNO3的溶解度曲线①在生产过程中,KNO3中混有少量KCl杂质,如果要在实验室中提纯KNO3晶体,应采用什么的方法?(杂质仅含KCl)②写出具体的实验方案。【提示】①降温结晶。②加热溶解KNO3样品,冷却结晶,过滤得到KNO3晶体,然后洗涤晾干。1.过滤实验应注意的3个问题2.两种常用的结晶方法蒸发结晶降温结晶原理利用加热的方法,使溶液中溶剂不断挥发而析出溶质(晶体)的过程通过降低...