第一章第一节元素周期表(3)【学习目标】1.了解原子结构与同位素、使学生懂得质量数和AZX的含义
2.初步学会元素周期表的位置与元素组成微粒的结构联系起来运用能力
【学习重点】同位素、质量数和AZX的含义【预备知识】原子的构成:原子看表分析:质量/kg相对质量电性和电量/C质子1.673×10-271.007+1.602×10-19中子1.675×10-271.0080电子9.109×10-311/1836-1.602×10-191、构成原子粒子所带的电性及电荷大小
2、质子带正电,电子带负电,而原子不显电性的原因
3、原子的质量主要取决于哪种微粒
总结:原子是由居于原子中心的带正电的和核外带负电的构成的
原子核由和构成
【基础知识】(一)质量数定义符号:计算式:质量数(A)=+应用:用质量数表示某种原子[思考]:它表示的含义是什么
[科学探究]:1、填写下表,总结A与相对原子质量的关系
原子质子数(Z)中子数(N)质子数+中子数(A)相对原子质量F1018.998Na1222.990Al1426.9822、原子形成离子之后构成原子的微粒哪些发生了变化
[总结和比较]:和中的质子数、中子数、质量数和电子数
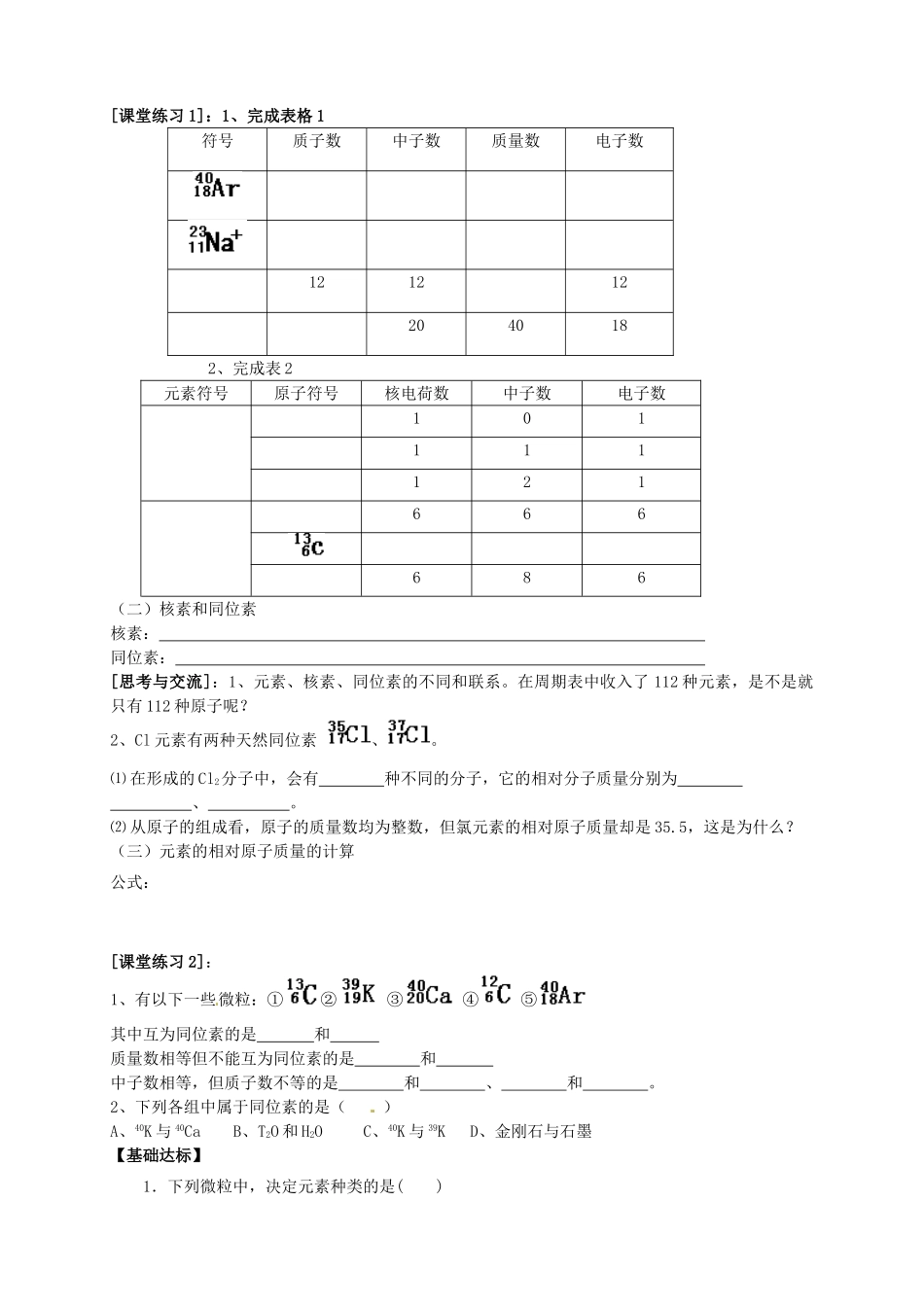
[课堂练习1]:1、完成表格1符号质子数中子数质量数电子数1212122040182、完成表2元素符号原子符号核电荷数中子数电子数101111121666686(二)核素和同位素核素:同位素:[思考与交流]:1、元素、核素、同位素的不同和联系
在周期表中收入了112种元素,是不是就只有112种原子呢
2、Cl元素有两种天然同位素、
⑴在形成的Cl2分子中,会有种不同的分子,它的相对分子质量分别为、
⑵从原子的组成看,原子的质量数均为整数,但氯元素的相对原子质量却是35
5,这是为什么
(三)元素的相对原子质量的计算公式:[课堂练习2]:1、有以下一些微