阐述硫铁矿为原料制取硫酸的主要工序及焙烧原理,并写出主要化学反应式
(10分)接触法硫酸生产过程⑴选矿:原料破碎、筛分、配料或干燥;⑵硫铁矿焙烧;⑶炉气净化;⑷SO2催化氧化;⑸炉气干燥和SO3吸收;⑹尾气回收SO2和污水处理
焙烧原理第一步是硫铁矿中的有效成分FeS2受热分解(高于400℃)成FeS和单体硫
这一步是吸热反应,温度越高对FeS2分解反应越有利
2FeS2=2FeS+S2第二步是分解出的单体硫与空气燃烧,生成SO2S2+2O2=2SO2硫铁矿在释出硫磺后,剩下的硫化铁在氧分压为3
04kPa以上时,生成红棕色的Fe2O3FeS+7O2=2Fe2O3+4SO2当氧含量在1%左右时,则生成棕黑色的Fe3O43FeS+5O2=Fe3O4+3SO2主要反应总反应方程式:4FeS2+11O2=8SO2+2Fe2O33FeS2+8O2=6SO2+Fe3O4副反应:2FeS2+7O2=Fe2(SO4)3+SO2硫铁矿中所含Cu、Pb、Zn、Co、Cd、As、Se等的硫化物,在焙烧后一部分成为氧化物2
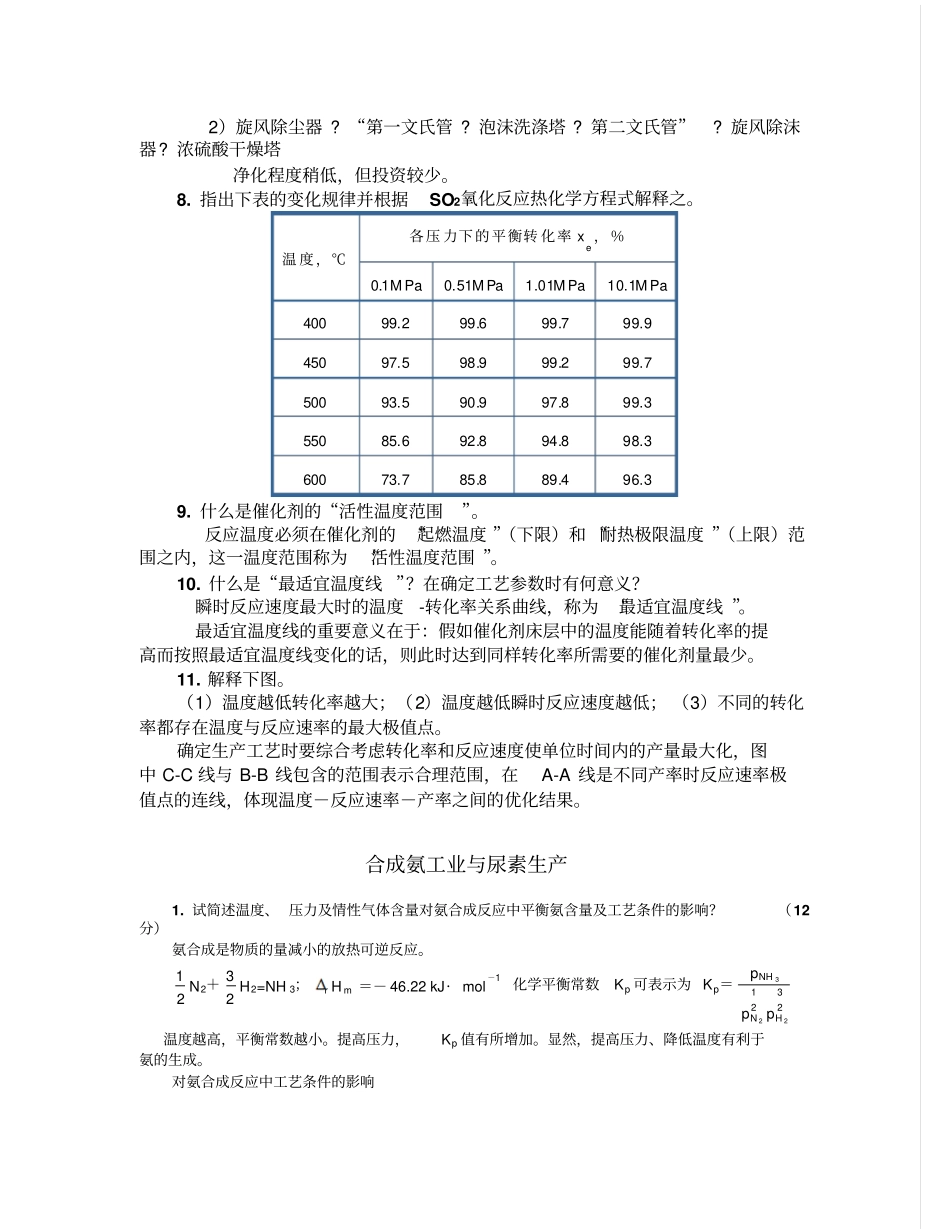
SO2催化氧化工艺条件如何确定
(20分)一、温度放热反应,降低温度,平衡转化率提高
反应速率随温度升高而迅速增大
催化剂有极限温度(起燃温度)和耐热极限温度(活性温度),范围在420℃~600℃
确定SO2转化反应温度的原则:在催化剂活性温度范围内,催化剂床层温度应尽量沿着最佳温度线变化,此时达到同样转化率所需催化剂量最少
这就要求原料气需预热至催化剂的起燃温度,然后随着反应的进行,适当移走多于的反应热,使床层温度尽可能地沿着最佳值变化
特别在反应后期,为了达到高的SO2转化率,反应必须在较低温度下进行
因此SO2转化反应及工业上多数可逆放热反应过程,总是与换热过程联系在一起
二、SO2原始浓度随着SO2浓度增加,O2浓度相应地下降,这两个因素都会使反应速率下降