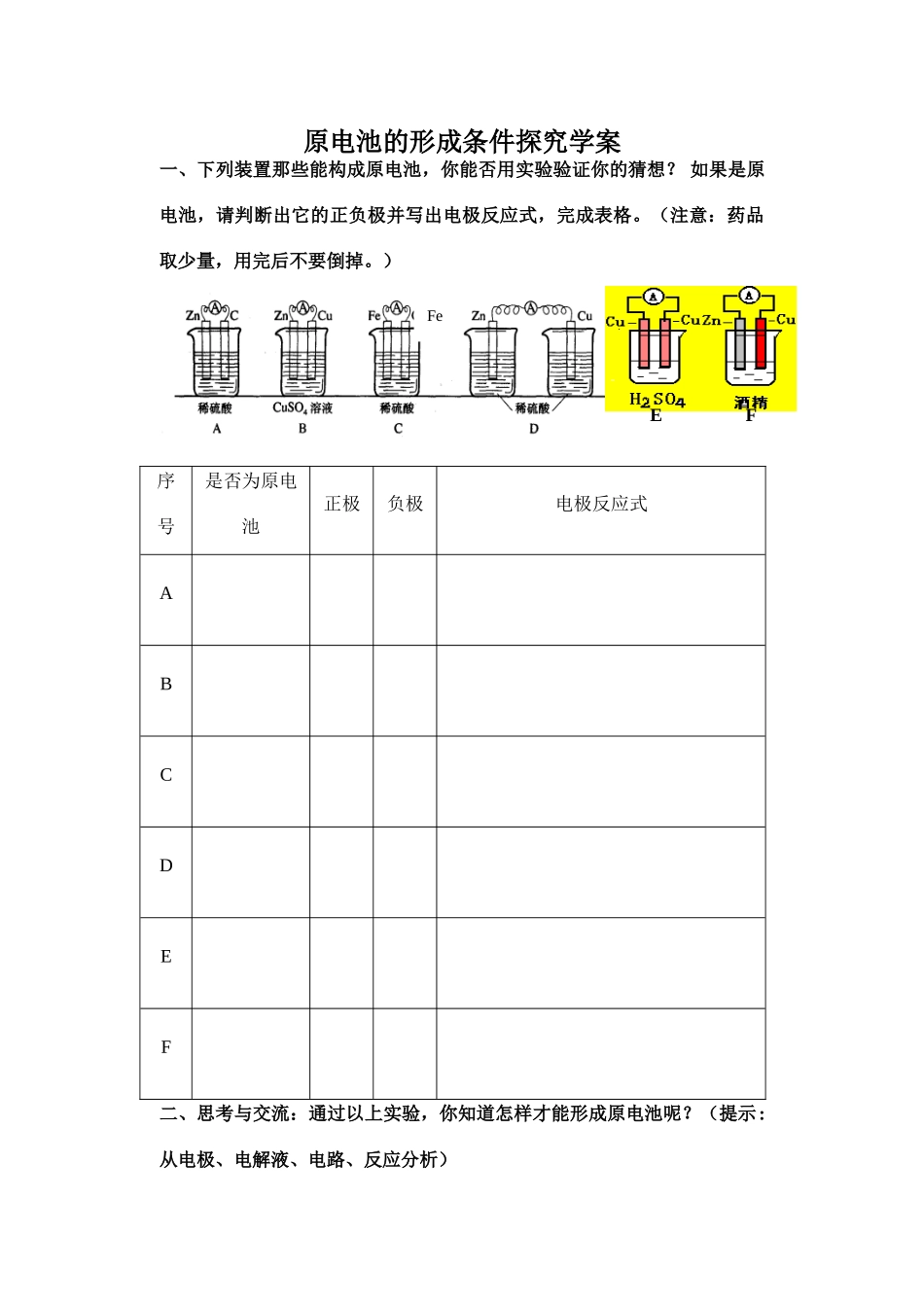
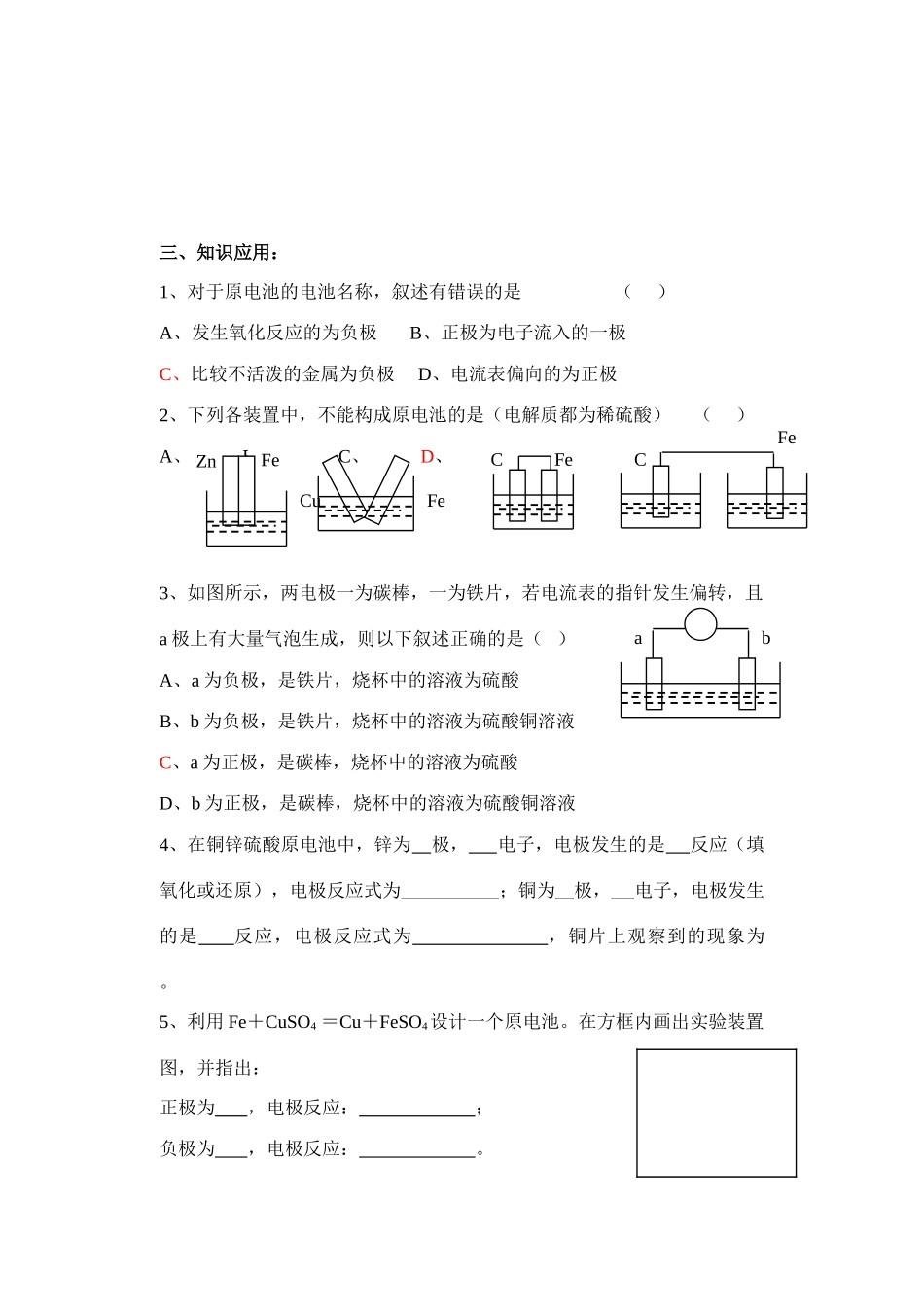
原电池的形成条件探究学案一、下列装置那些能构成原电池,你能否用实验验证你的猜想
如果是原电池,请判断出它的正负极并写出电极反应式,完成表格
(注意:药品取少量,用完后不要倒掉
)序号是否为原电池正极负极电极反应式ABCDEF二、思考与交流:通过以上实验,你知道怎样才能形成原电池呢
(提示:从电极、电解液、电路、反应分析)EFFe三、知识应用:1、对于原电池的电池名称,叙述有错误的是()A、发生氧化反应的为负极B、正极为电子流入的一极C、比较不活泼的金属为负极D、电流表偏向的为正极2、下列各装置中,不能构成原电池的是(电解质都为稀硫酸)()A、B、C、D、3、如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是()A、a为负极,是铁片,烧杯中的溶液为硫酸B、b为负极,是铁片,烧杯中的溶液为硫酸铜溶液C、a为正极,是碳棒,烧杯中的溶液为硫酸D、b为正极,是碳棒,烧杯中的溶液为硫酸铜溶液4、在铜锌硫酸原电池中,锌为极,电子,电极发生的是反应(填氧化或还原),电极反应式为;铜为极,电子,电极发生的是反应,电极反应式为,铜片上观察到的现象为
5、利用Fe+CuSO4=Cu+FeSO4设计一个原电池
在方框内画出实验装置图,并指出:正极为,电极反应:;负极为,电极反应:
FeCFeCFeCuFeZnbaCuFeFeCZn6、已知电极材料:铁、铜、银、石墨、锌、铝;电解质溶液:CuCl2溶液Fe2(S04)3溶液、盐酸
按要求回答下列问题:(1)电工操作上规定:不能把铜导线和铝导线连接在一起使用
请说明原因(2)若电极材料选铜和石墨,电解质溶液选硫酸铁溶液,外加导线,能否构成原电池
,若能,请写出电极反应式,负极_,正极
(若不能,后面两空不填)答案1、C、2、D、3、C4、负极,失去,氧化,Zn-2e—=Zn2+;正极,得到,还原,2H