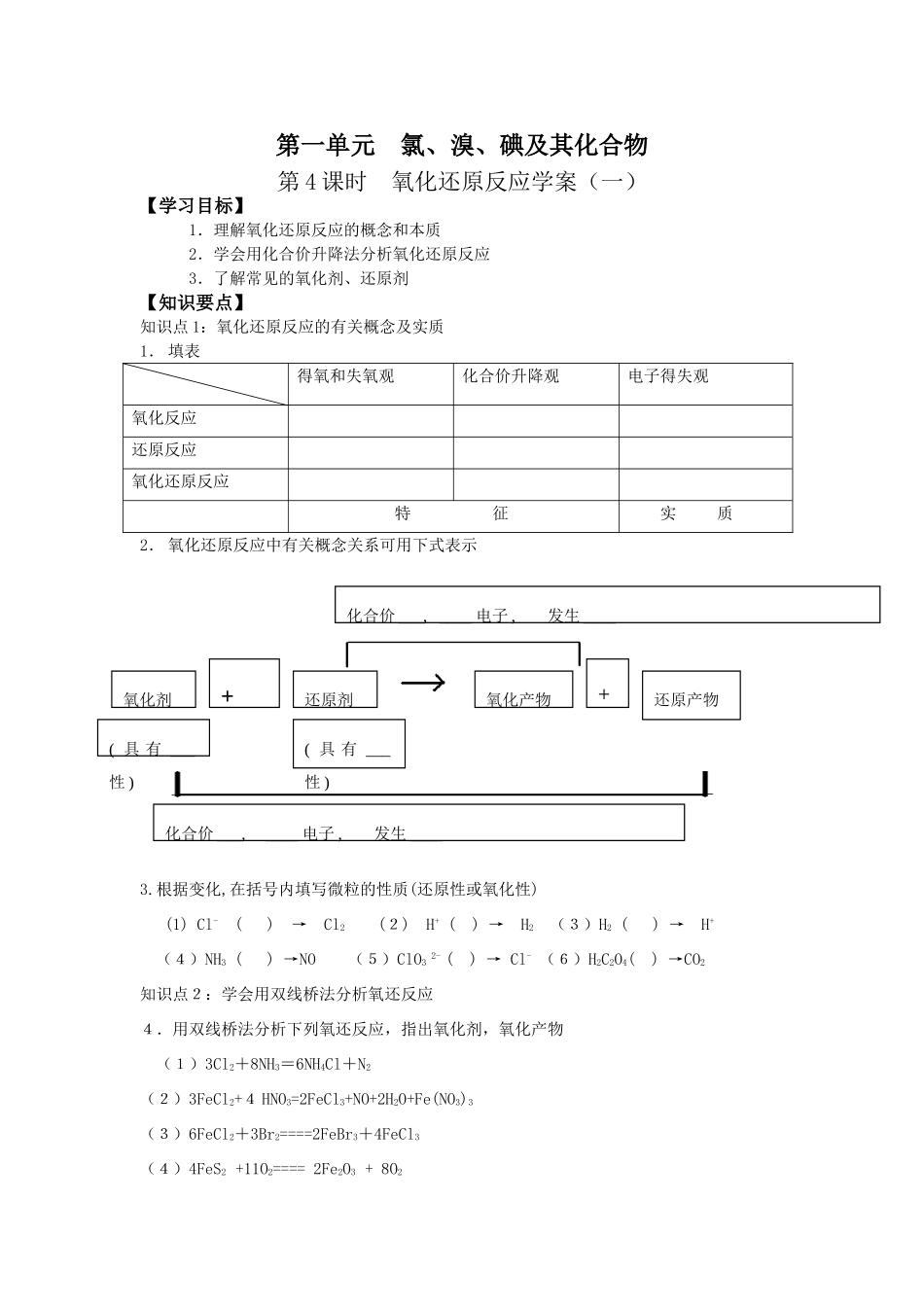
第一单元氯、溴、碘及其化合物第4课时氧化还原反应学案(一)【学习目标】1.理解氧化还原反应的概念和本质2.学会用化合价升降法分析氧化还原反应3.了解常见的氧化剂、还原剂【知识要点】知识点1:氧化还原反应的有关概念及实质1.填表得氧和失氧观化合价升降观电子得失观氧化反应还原反应氧化还原反应特征实质2.氧化还原反应中有关概念关系可用下式表示3
根据变化,在括号内填写微粒的性质(还原性或氧化性)(1)Cl-()→Cl2(2)H+()→H2(3)H2()→H+(4)NH3()→NO(5)ClO32-()→Cl-(6)H2C2O4()→CO2知识点2:学会用双线桥法分析氧还反应4.用双线桥法分析下列氧还反应,指出氧化剂,氧化产物(1)3Cl2+8NH3=6NH4Cl+N2(2)3FeCl2+4HNO3=2FeCl3+NO+2H2O+Fe(NO3)3(3)6FeCl2+3Br2====2FeBr3+4FeCl3(4)4FeS2+11O2====2Fe2O3+8O2(具有___性)氧化剂还原剂氧化产物还原产物(具有___性)化合价___,____电子,发生____化合价___,____电子,发生____++5.在反应K2Cr2O7+14HCl====2KCl+2CrO3+3Cl2+7H2O中若有2moLK2Cr2O7参加反应则被氧化的HCl为____________mol转移电子_____________mol参加反应的HCl_________mol知识点3:氧化还原反应与其它反应类型的关系知识点4:常见氧化剂,还原剂6.常见氧化剂有:<1>活泼的非金属单质:_____________________________<2>含高价态元素的化合物:_________________________常见还原剂有:<1>金属单质:_______________________<2>含较低价态元素