四川省宜宾市南溪二中高二化学(选修3)导学案:第一章第一节原子结构【学习目标】1、进一步认识原子核外电子的分层排布2、知道原子核外电子的能层、能级分布及其能量关系3、知道原子核外电子的排布遵循能量最低原理、泡利原理、洪特规则4、了解原子结构的构造原理,能用构造原理认识原子的核外电子排布能用电子排布式表示常见元素(1~36号)原子核外电子的排布【知识呈现】一、原子的诞生大爆炸宇宙学理论(H、He、Li→形成其他元素)现用周期表有种元素,其中非金属元素有种(如果继续完善应有种)二、能层、能级、轨道能层一(K)二(L)三(M)四(N)五(O)六(P)七(Q)能级1s2s2p3s3p3d4s4p4d4f5s5p5d5f5g……
各能级轨道数(n2)11+3=41+3+5=91+3+5+7=161+3+5+7+9=25………………
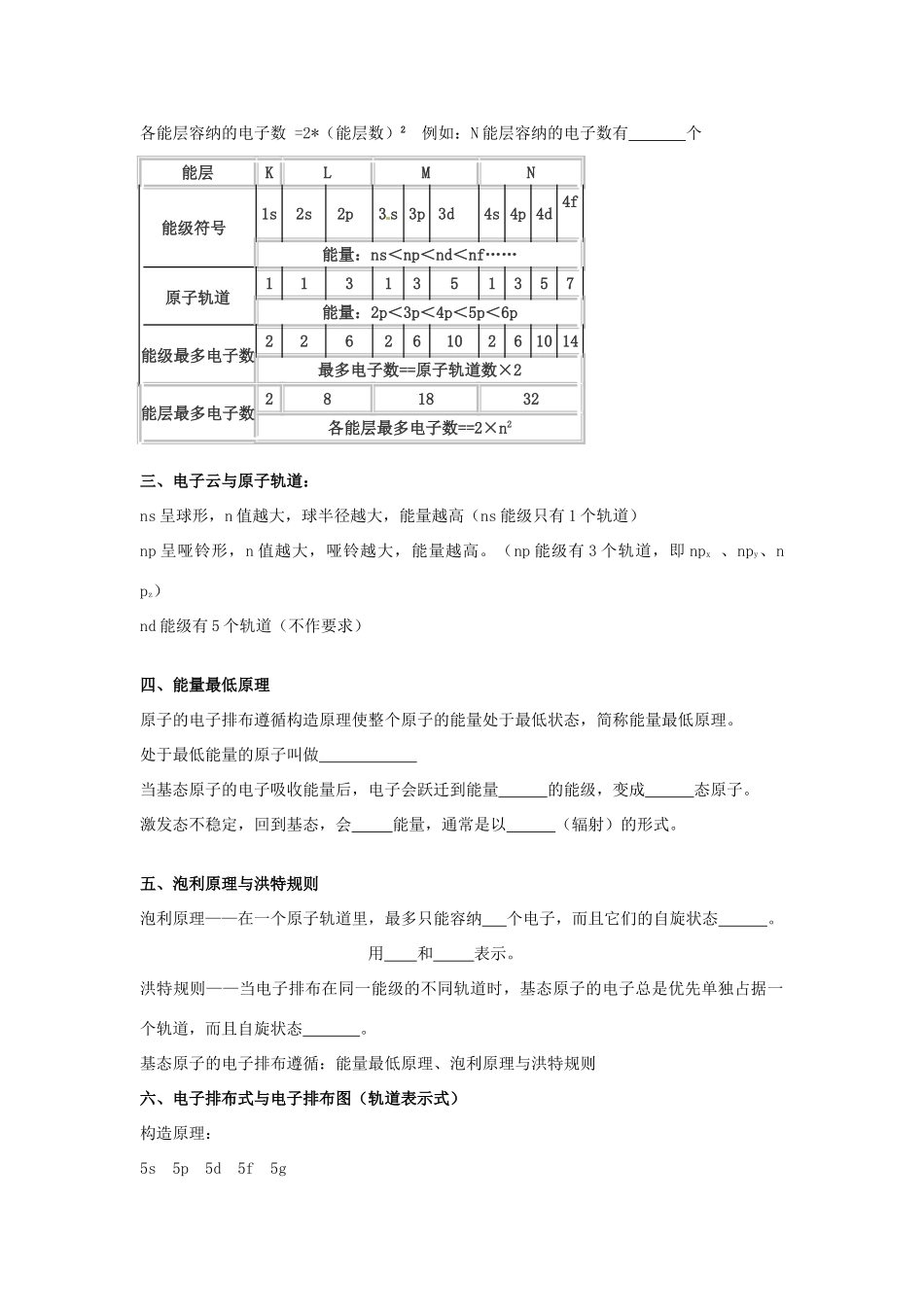
各能级可容纳电子数(2n2)22+6=82+6+10=182+6+10+14=322+6+10+14+18=50各能层的能级数=能层数例如:N能层有个能级,它们是各能层的轨道数=(能层数)2例如:N能层的轨道数有个各能层容纳的电子数=2*(能层数)2例如:N能层容纳的电子数有个能层KLMN能级符号[1s2s2p[3s3p3d[]4s4p4d4fm]能量:ns<np<nd<nf……原子轨道1131351357能量:2p<3p<4p<5p<6p能级最多电子数2262610261014最多电子数==原子轨道数×2能层最多电子数281832各能层最多电子数==2×n2三、电子云与原子轨道:ns呈球形,n值越大,球半径越大,能量越高(ns能级只有1个轨道)np呈哑铃形,n值越大,哑铃越大,能量越高
(np能级有3个轨道,即npx、npy、npz)nd能级有5个轨道(不作要求)四、能量最低原理原子的电子排布遵循构造原理使整个原子的能量处于最低状态,简称能