八、高中化学教材常考实验总结(一)配制一定物质的量浓度的溶液1
注意事项(1)容量瓶:只有一个刻度线,只能配制瓶上规定容积的溶液,若配制480mL溶液应用500mL容量瓶
(2)写所用仪器时,容量瓶必须注明规格
(3)容量瓶使用之前必须查漏
误差分析依据:cB==
命题角度:一是仪器的缺失与选择,二是实验误差分析
(二)Fe(OH)2的制备1
实验现象:白色沉淀迅速转化灰绿色,最后变成红褐色沉淀
反应方程式为:Fe2++2OH-===Fe(OH)2↓4Fe(OH)2+O2+2H2O===4Fe(OH)3
注意事项:Fe(OH)2具有较强的还原性,容易被氧化
(1)所用亚铁盐溶液必须是新制的,NaOH溶液必须煮沸;(2)胶头滴管须插入试管底部;(3)往往在液面加一层油膜,如少量煤油、苯或植物油等;或用如图所示改进装置
命题角度:制备过程中的现象、创设无氧环境
(三)氨气的实验室制法1
反应原理:2NH4Cl+Ca(OH)2=====CaCl2+2NH3↑+2H2O
气体制备流程:原理——发生装置——除杂干燥——收集——验满——尾气处理
注意事项(1)制备装置中试管口要低于试管底、收集装置中导管应插入试管底部
(2)浓氨水(或浓铵盐溶液)滴到生石灰或烧碱中制氨气,或浓氨水直接加热也可制氨气
(3)不能使用NH4Cl和NH4HCO3制备
命题角度:物质制备原理、发生装置、除杂干燥、收集、尾气处理等,并以此基础进行性质探究实验
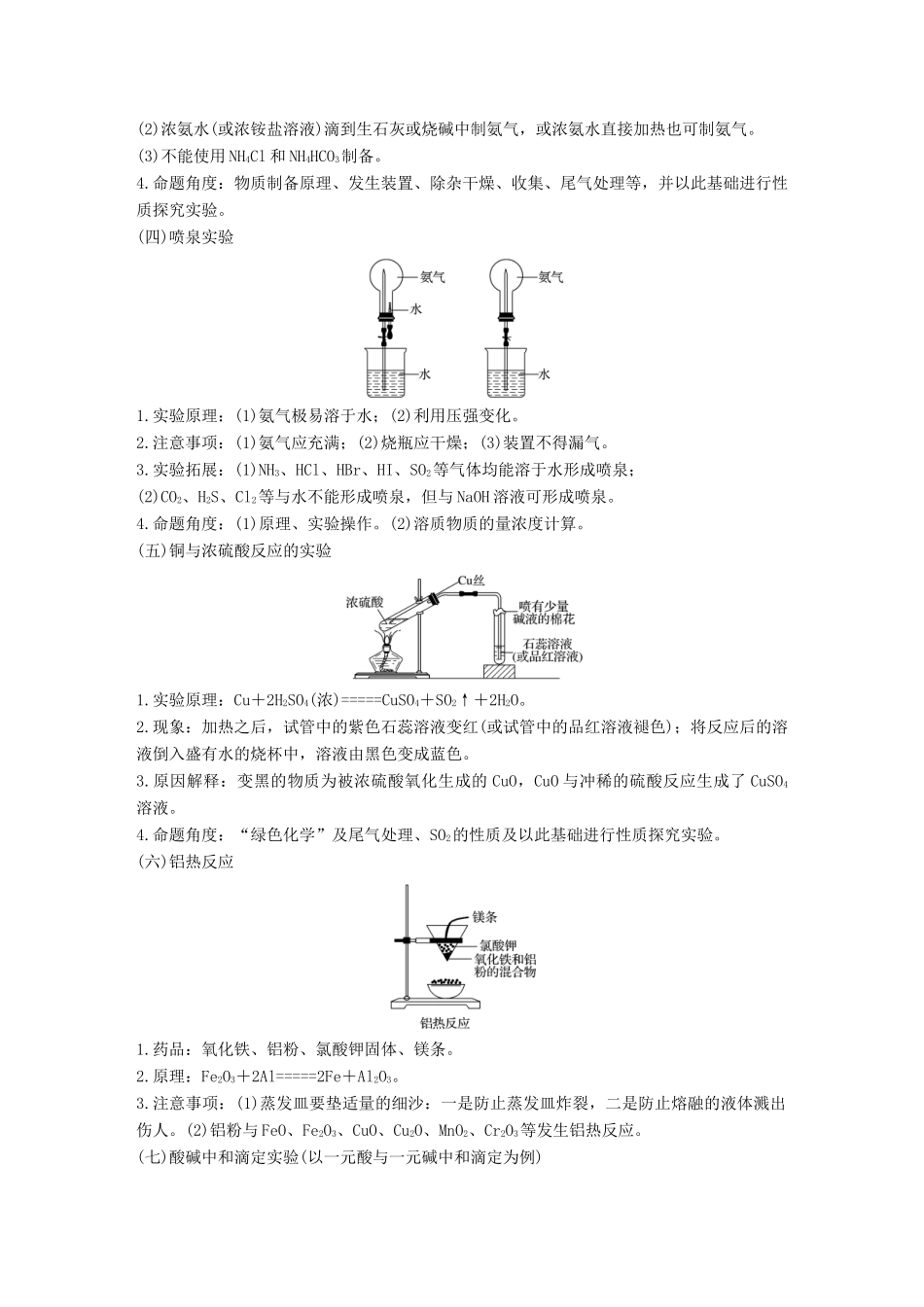
(四)喷泉实验1
实验原理:(1)氨气极易溶于水;(2)利用压强变化
注意事项:(1)氨气应充满;(2)烧瓶应干燥;(3)装置不得漏气
实验拓展:(1)NH3、HCl、HBr、HI、SO2等气体均能溶于水形成喷泉;(2)CO2、H2S、Cl2等与水不能形成喷泉,但与NaOH溶液可形成喷泉
命题角度:(1