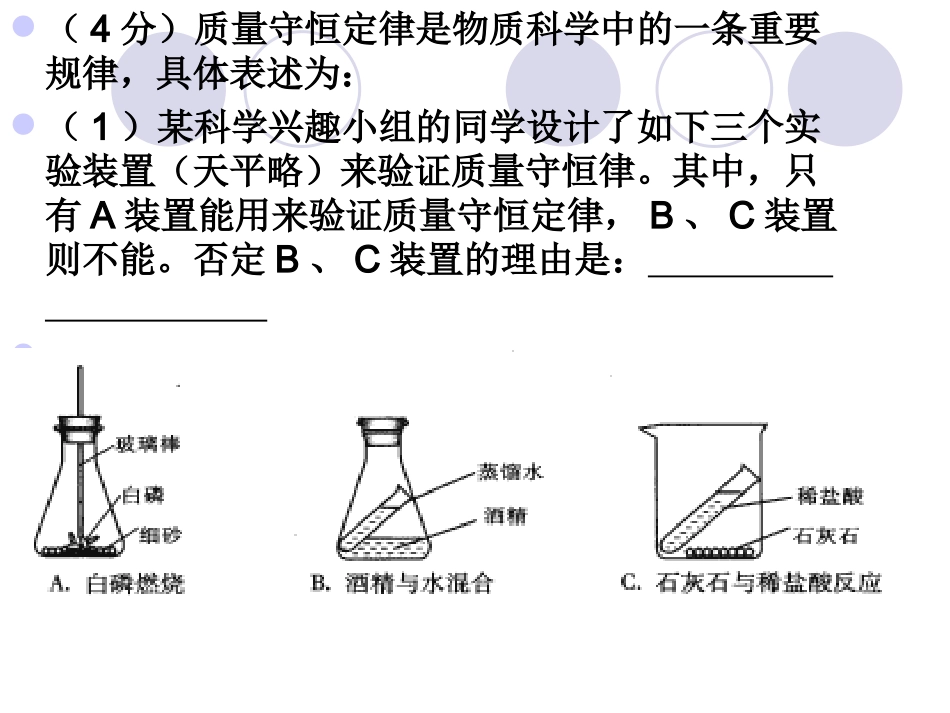
总体目标:1、能正确说出质量守恒定律2、知道化学反应应遵循质量守恒定律的原因3、能用质量守恒定律解释常见的化学变化的质量关系4、能用最小公倍数法配平简单的化学方程式5、会书写简单的化学方程式6、能利用化学方程式进行简单的化学计算(4分)质量守恒定律是物质科学中的一条重要规律,具体表述为:(1)某科学兴趣小组的同学设计了如下三个实验装置(天平略)来验证质量守恒律
其中,只有A装置能用来验证质量守恒定律,B、C装置则不能
否定B、C装置的理由是:
(2)小明将C装置进行改进,如图D所示
①此实验的现象是
②待完全反应后,将装置D置于天平上称量,所得数据较反应前的小
若整个操作过程无差错,则造成上述实验误差的原因是
一、质量守恒定律是自然界的客观规律1质量守恒定律的内容:
2质量守恒的原因
3在化学反应中量的变化情况(5不变两变一可能变)参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,反应前后的原子种类没有改变,原子的数目没有增减,原子的质量也没有变化
2、质量守恒定律的解释可总结为五个不变,两个改变,一个可能改变宏观反应物和生成物的总质量元素的质量和种类不变微观原子的种类不变原子的数目不变原子的质量不变两个一定改变五个不变宏观微观物质种类改变一个可能改变:分子总数可能改变分子的种类3)已知反应,则X的化学式为
OHCOOX222223点燃4)亚硝酸钠(NaNO2)能分解放出刺激性气味气体的是亚硝酸钠,此气体可能是()A、SO2B、NH3C、N2D、NO2A5如图是某化学反应的微观示意图,其中不同的圆球代表不同原子
下列说法中正确的是()A.该反应涉及到四种原子B.该反应属于分解反应C.参加反应的两种分子的个数比为1∶1D.该反应前后所有元素的化合价都没有变化(反应前)(反应后)→催化剂C2H4DC(反应前)(反应后)→催化剂5