第三章金属及其化合物第一节金属的化学性质【本节学习要点】1.了解钠、铝的物理性质
2.以Na、Mg、Al、Fe为例,掌握金属与O2等非金属的反应,通过Na与O2反应的学习,明确反应条件不同,反应现象及反应产物也不同
3.通过Na与水反应,Fe与水蒸气反应,Al与NaOH溶液反应,活泼金属与酸反应,掌握金属与酸和水的反应
4.掌握物质的量在化学方程式计算中的应用
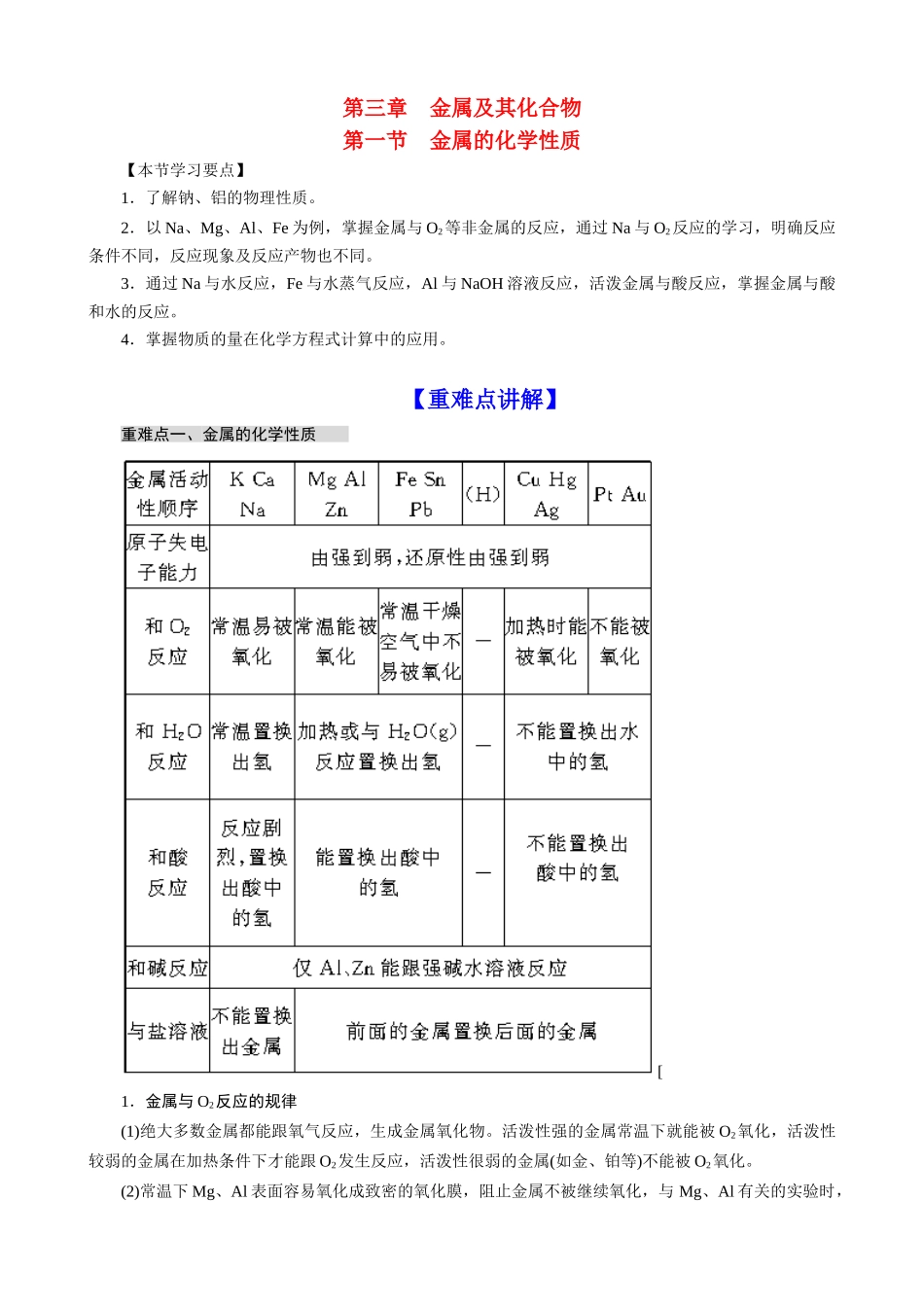
【重难点讲解】重难点一、金属的化学性质[1.金属与O2反应的规律(1)绝大多数金属都能跟氧气反应,生成金属氧化物
活泼性强的金属常温下就能被O2氧化,活泼性较弱的金属在加热条件下才能跟O2发生反应,活泼性很弱的金属(如金、铂等)不能被O2氧化
(2)常温下Mg、Al表面容易氧化成致密的氧化膜,阻止金属不被继续氧化,与Mg、Al有关的实验时,要注意除去表面的氧化膜
(3)部分金属与O2反应的产物与条件有关
如:Fe在不同条件下与O2可以生成FeO、Fe2O3或Fe3O4
铁在O2中燃烧生成Fe3O4
铁生锈时生成Fe2O3·nH2O
再如:Na在常温下生成Na2O,加热时生成Na2O2
2.金属与水反应的一般规律(1)活泼金属如K、Ca、Na可与冷水迅速剧烈反应(放热反应)生成H2
2K+2H2O===2KOH+H2↑(2)较活泼金属与冷水不反应,可与沸水或H2O(g)反应
Mg与冷水反应缓慢,但加热水后(或沸水),Mg与水的反应加快,Mg+2H2O=====Mg(OH)2+H2↑Al在沸水条件下反应缓慢,2Al+6H2O=====2Al(OH)3+3H2↑高温下,Zn、Fe、Sn、Pb和水蒸气可以反应生成金属氧化物和H2
(3)氢后金属不能置换出H2O中的氢
氢前金属在一定条件下可置换出水中的氢
特别提醒Fe与H2O反应为置换反应,氧化产物为Fe3O4,而不是Fe2O3
3.金属与酸反应规律金属活动顺序表中位于氢之前