第1课时弱电解质的电离平衡[学习目标定位]1
会描述弱电解质的电离平衡,能正确书写弱电解质的电离方程式,会分析电离平衡的移动
知道电离平衡常数的意义
一、弱电解质的电离平衡1
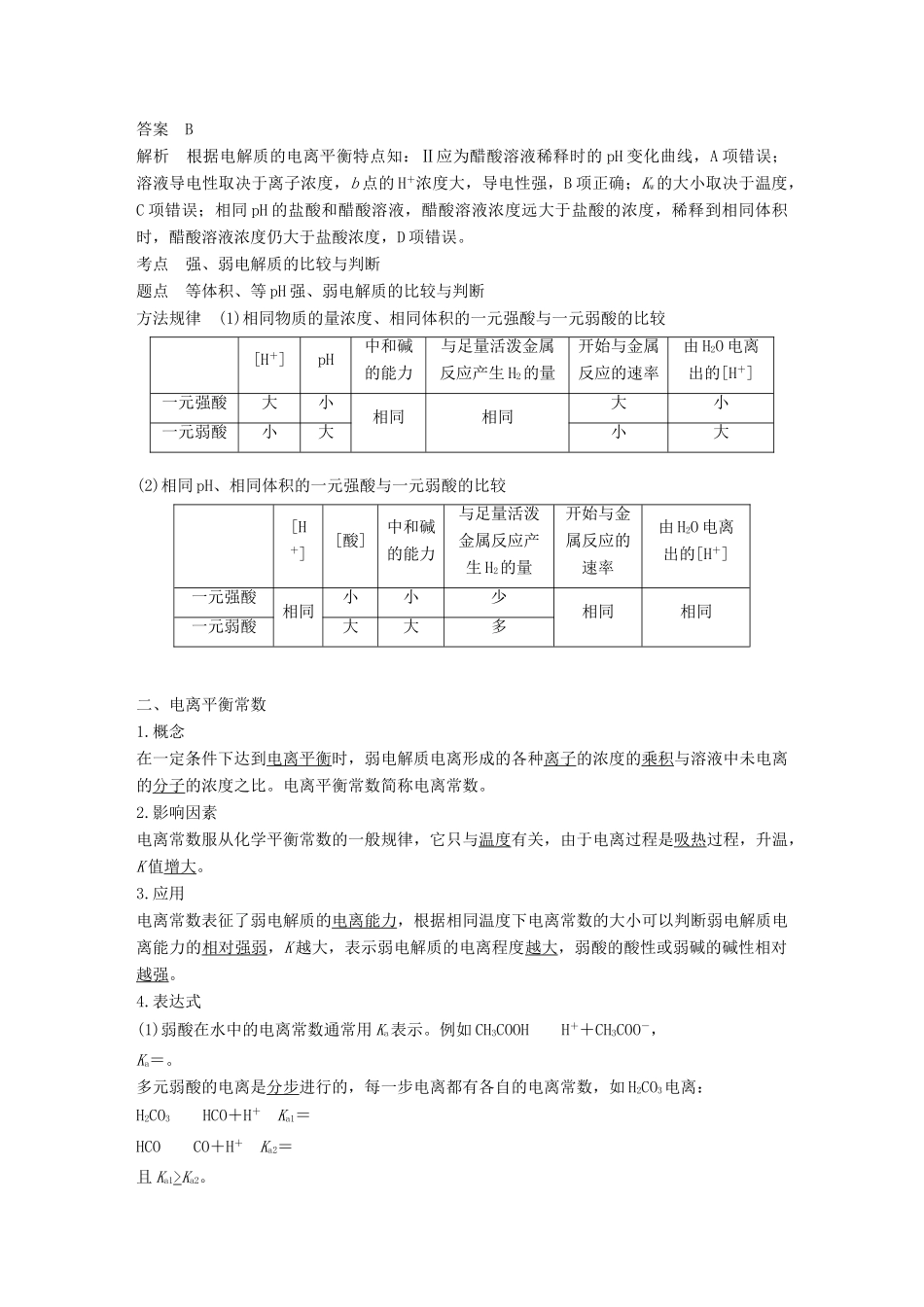
弱电解质电离平衡的建立过程如图是醋酸溶于水时,电离过程中,醋酸分子电离成离子的速率、离子重新结合成醋酸分子的速率随时间的变化曲线
请回答下列问题:va表示醋酸分子电离成离子的速率;vb表示离子结合成醋酸分子的速率
(1)在时间由t0到t1过程中,va的变化是不断减小,vb的变化是不断增大
(2)当时间达t1后,va与vb的关系是va=vb≠0,此时醋酸达到电离平衡状态
(3)分析醋酸电离过程中,溶液中各粒子浓度的变化,填写下表:粒子浓度[H+][CH3COO-][CH3COOH]醋酸初溶于水接近于0接近于0最大达到电离平衡前增大增大减小达到电离平衡时不变不变不变2
电离平衡的概念与特征(1)在一定条件(如温度、浓度)下,当弱电解质分子电离成离子的速率和离子重新结合成弱电解质分子的速率相等时,电离过程就达到了电离平衡状态
(2)弱电解质的电离平衡是一种动态平衡,平衡时其电离过程并没有停止,只是溶液中各分子和离子的浓度都保持不变
影响电离平衡的因素以醋酸的电离平衡为例,分析改变下列条件对醋酸电离平衡的影响,填写下表:条件改变平衡移动方向[H+]n(H+)电离程度导电能力升高温度向右移动增大增大增大增强加H2O向右移动减小增大增大减弱通HCl向左移动增大增大减小增强加少量NaOH(s)向右移动减小减小增大增强加少量CH3COONa(s)向左移动减小减小减小增强加少量CH3COOH向右移动增大增大减小增强影响电离平衡的因素(1)内因弱电解质本身的性质,如相同条件下CH3COOH电离程度大于H2CO3
(2)外因①温度:升高温度,电离平衡向电离方向移动;降低温度,电离平衡向逆电离方向移动
②浓度:改变平