第2课时共价键的键能与化学反应的反应热、原子晶体(时间:30分钟)考查点一共价键的键能与反应热1
下列说法中正确的是()
双原子分子中化学键键能越大,分子越稳定B
双原子分子中化学键键长越长,分子越稳定C
双原子分子中化学键键角越大,分子越稳定D
在双键中,σ键的键能要小于π键的解析在双原子分子中没有键角,故C错
当其键能越大,键长越短时,分子越稳定,故A对,B错
D中σ键的重叠程度要大于π键的,故σ键的键能要大于π键的
能够用键能的大小作为主要依据来解释的是()
常温常压下氯气呈气态而溴单质呈液态B
硝酸是挥发性酸,而硫酸、磷酸是不挥发性酸C
稀有气体一般难于发生化学反应D
空气中氮气的化学性质比氧气稳定解析共价分子构成物质的状态取决于分子间作用力的大小,与分子内共价键的键能无关;物质的挥发性与分子内键能的大小无关;稀有气体是单原子分子,无化学键,难于发生化学反应的原因是它们的价电子已形成稳定结构;氮气比氧气稳定是由于N2分子中形成共价键的键能(946kJ·mol-1)比O2分子中共价键的键能(497
3kJ·mol-1)大,在化学反应中更难断裂
下列过程中,共价键被破坏的是()
溴蒸气被活性炭吸附C
蔗糖溶于水D
SO2溶于水解析碘升华、溴蒸气被活性炭吸附和蔗糖溶于水破坏的是范德华力,SO2溶于水,与H2O反应生成H2SO3,共价键被破坏,形成新的共价键
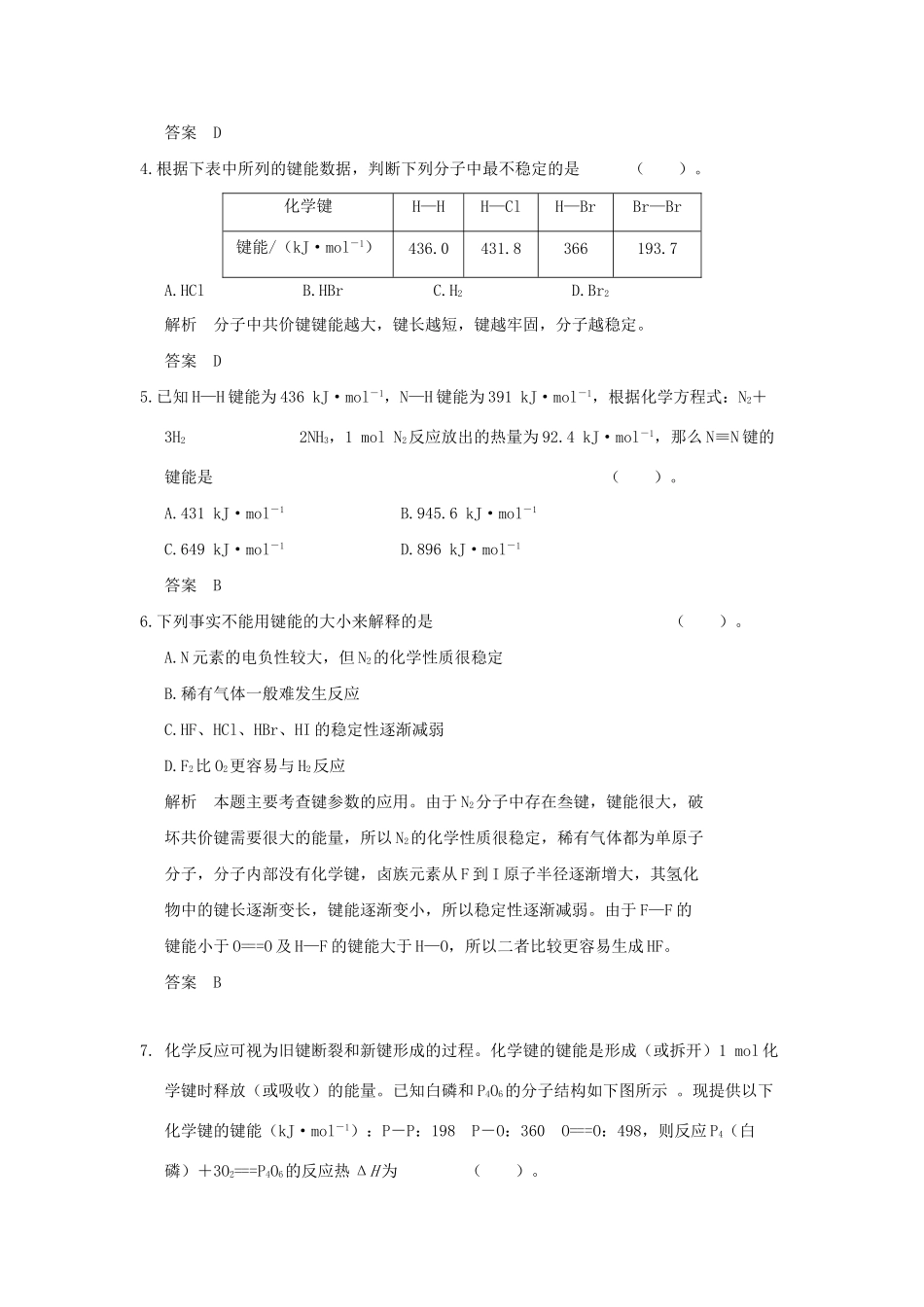
根据下表中所列的键能数据,判断下列分子中最不稳定的是()
化学键H—HH—ClH—BrBr—Br键能/(kJ·mol-1)436
8366193
Br2解析分子中共价键键能越大,键长越短,键越牢固,分子越稳定
已知H—H键能为436kJ·mol-1,N—H键能为391kJ·mol-1,根据化学方程式:N2+3H2