山东省泰安市肥城市第三中学高中化学元素周期律和元素周期表(第一课时)学案鲁科版必修2学习内容学习目标:采用归纳总结的方法引导学生探索元素的性质(元素原子最外层电子排布、原子半径以及主要化合价、原子得失电子能力)和原子结构的关系从而归纳出元素周期律,揭示元素周期律的实质学习重点:元素的性质与原子结构的关系学习难点:元素的性质与原子结构的关系学习指导即时感悟【回顾﹒预习】1、原子序数:在数值上:原子序数=2、完成课本11---12页的内容
对于第二小题学习小组中A1B1C1利用柱状图完成,A2B2C2利用折线图完成
总结规律:1、2、3、【自主﹒合作﹒探究】探究一观察总结]仔细观察预习作业,讨论后总结规律如下表1:原子序数电子层数最外层电子数达到稳定结构时最外层电子数1~23~1011~18结论:
(图见书P11)
自我完成,回顾知识
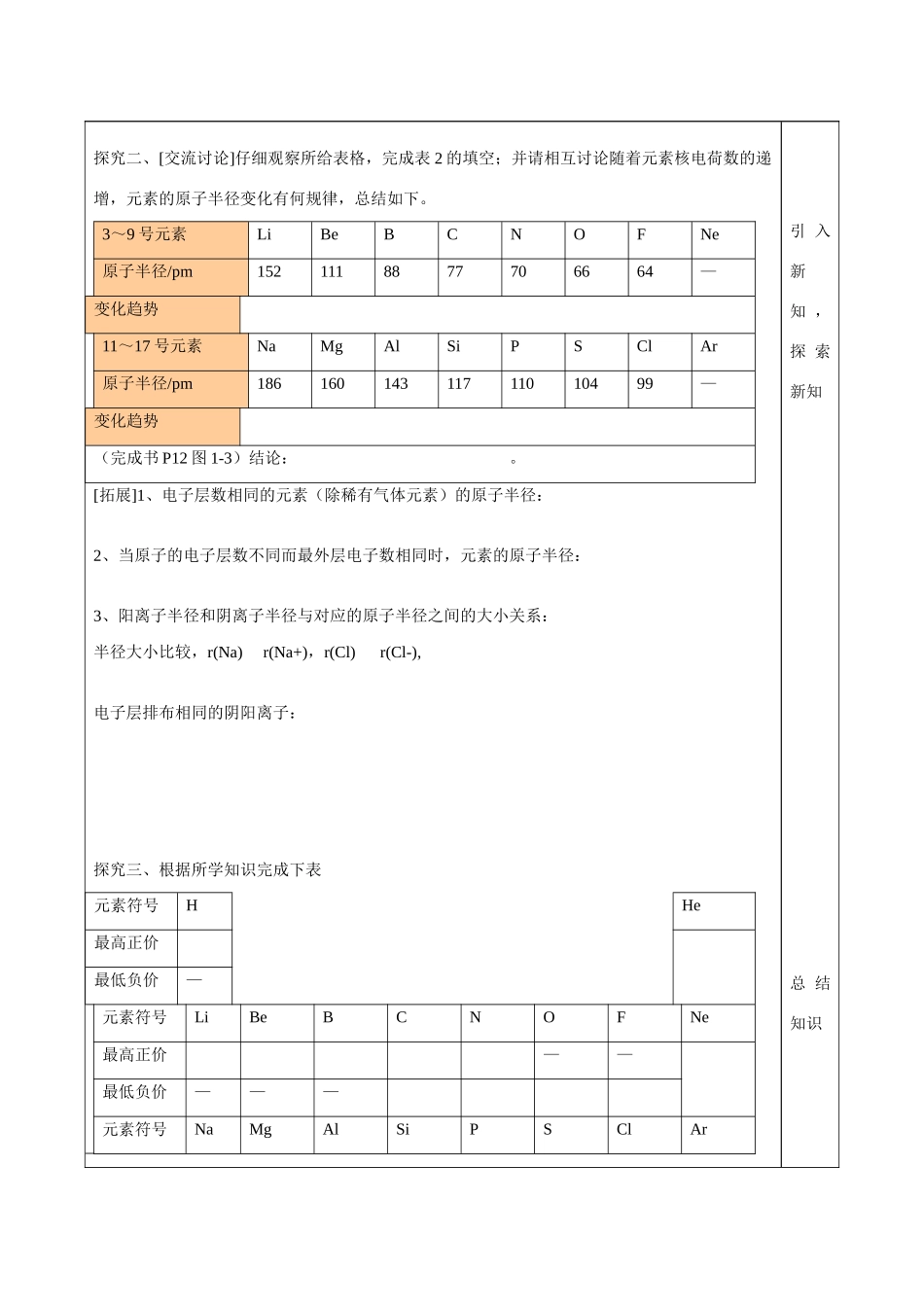
了解新知探究二、[交流讨论]仔细观察所给表格,完成表2的填空;并请相互讨论随着元素核电荷数的递增,元素的原子半径变化有何规律,总结如下
3~9号元素LiBeBCNOFNe原子半径/pm1521118877706664—变化趋势11~17号元素NaMgAlSiPSClAr原子半径/pm18616014311711010499—变化趋势(完成书P12图1-3)结论:
[拓展]1、电子层数相同的元素(除稀有气体元素)的原子半径:2、当原子的电子层数不同而最外层电子数相同时,元素的原子半径:3、阳离子半径和阴离子半径与对应的原子半径之间的大小关系:半径大小比较,r(Na)r(Na+),r(Cl)r(Cl-),电子层排布相同的阴阳离子:探究三、根据所学知识完成下表元素符号HHe最高正价最低负价—元素符号LiBeBCNOFNe最高正价——最低负价———元素符号NaMgAlSiPSClAr引入新知,探索新知总结知识最高正价最低负价———原子序数为11~17的元