专题重要无机物的知识发散(建议课时:3课时)元素化合物知识在高考试卷中,贯穿始终,题型灵活,其出现的频数之高、作用之大、运用之广,很直接地反映出了其在知识体系中的重要性
而且元素化合物的知识不仅是试题要直接考查的内容的本身,更是用来解决其他相关问题的基础和平台,学生解题的很多困难往往就是在对这些基本知识的理解、记忆和应用的方面达不到基本的要求,这是我们在复习中需要十分关注的问题
专项突破一重要代表物的转化、性质与应用物质1钠及其重要化合物1.性质(1)转化反应①离子方程式:2Na+2H2O===2Na++2OH-+H2↑;②化学方程式:2Na+O2=====Na2O2;③离子方程式:2Na2O2+2H2O===4Na++4OH-+O2↑;④化学方程式:2Na2O2+2CO2===2Na2CO3+O2;⑤化学方程式:2NaHCO3=====Na2CO3+CO2↑+H2O;⑥离子方程式:2OH-+CO2===CO+H2O;⑦离子方程式:CO2+OH-===HCO;⑧化学方程式:2NaCl+2H2O=====2NaOH+H2↑+Cl2↑
(2)拓展反应①Na制备Ti:4Na+TiCl4=====4NaCl+Ti
②Na与CuSO4溶液反应的离子方程式:2Na+2H2O+Cu2+===2Na++Cu(OH)2↓+H2↑
③Na与盐酸反应:2Na+2HCl===2NaCl+H2↑
④Na2O2和SO2的反应:Na2O2+SO2===Na2SO4
⑤NaHCO3与过量Ca(OH)2溶液反应的离子方程式:HCO+Ca2++OH-===CaCO3↓+H2O
⑥NaHCO3与少量Ca(OH)2溶液反应的离子方程式:2HCO+Ca2++2OH-===CaCO3↓+CO+2H2O
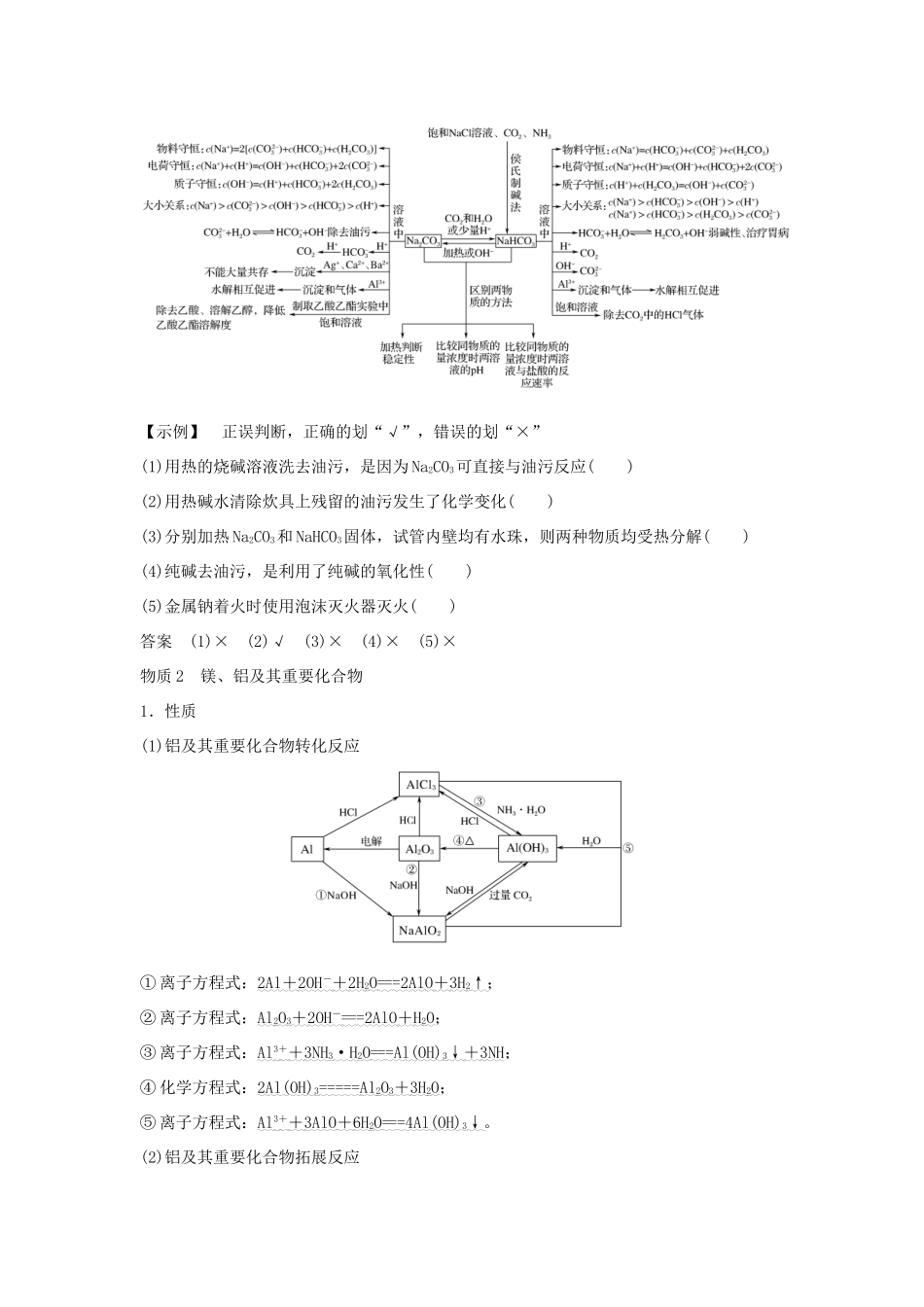
2.钠及其重要化合物的应用物质日常应用原因分析钠核反应堆的传热介质熔点较低,导热性好过氧化钠呼吸面具或潜水艇中作为氧