新课标人教版高中化学必修2第二章化学反应与能量全部教学案【课题】第一节化学能与热能(第1课时)9
28【教学目标】1、能从化学键的角度理解化学反应中能量变化的主要原因
2、能从微观的角度来解释宏观化学现象,进一步发展想象能力
3、通过化学能与热能的相互转变,理解“能量守恒定律”,初步建立起科学的能量观,加深对化学在解决能源问题中重要作用的认识
【重点难点】1
化学能与热能的内在联系及相互转变
从本质上理解化学反应中能量的变化,从而建立起科学的能量变化观
【教学过程】能源与材料、信息一起被称为现代社会发展的三大支柱
人类文明始于用火-----热能的使用,现代社会的一切活动都离不开能源,在影响全球经济和生活的各种因素中,能源居于首位
我们的日常生活中离不开能源,如液化气
它在燃烧时放出热能
那这些热能从何而来呢
本节课,我们将围绕这些问题,先从微观和宏观的角度来揭示这些秘密
[创设问题情景]氢气和氯气的混合气体遇到强光会发生什么现象
[教师补充讲解]化学反应的本质是反应物中化学键的断裂和生成物中化学键的形成
化学键是物质内部微粒之间强烈的相互作用,断开反应物中的化学键需要吸收能量,形成生成物中的化学键要放出能量
氢气和氯气反应的本质是在一定的条件下,氢气分子和氯气分子中的H-H键和Cl-Cl键断开,氢原子和氯原子通过形成H-Cl键而结合成HCl分子
1molH2中含有1molH-H键,1molCl2中含有1molCl-Cl键,在25℃和101kPa的条件下,断开1molH-H键要吸收436kJ的能量,断开1molCl-Cl键要吸收243kJ的能量,而形成1molHCl分子中的H-Cl键会放出431kJ的能量
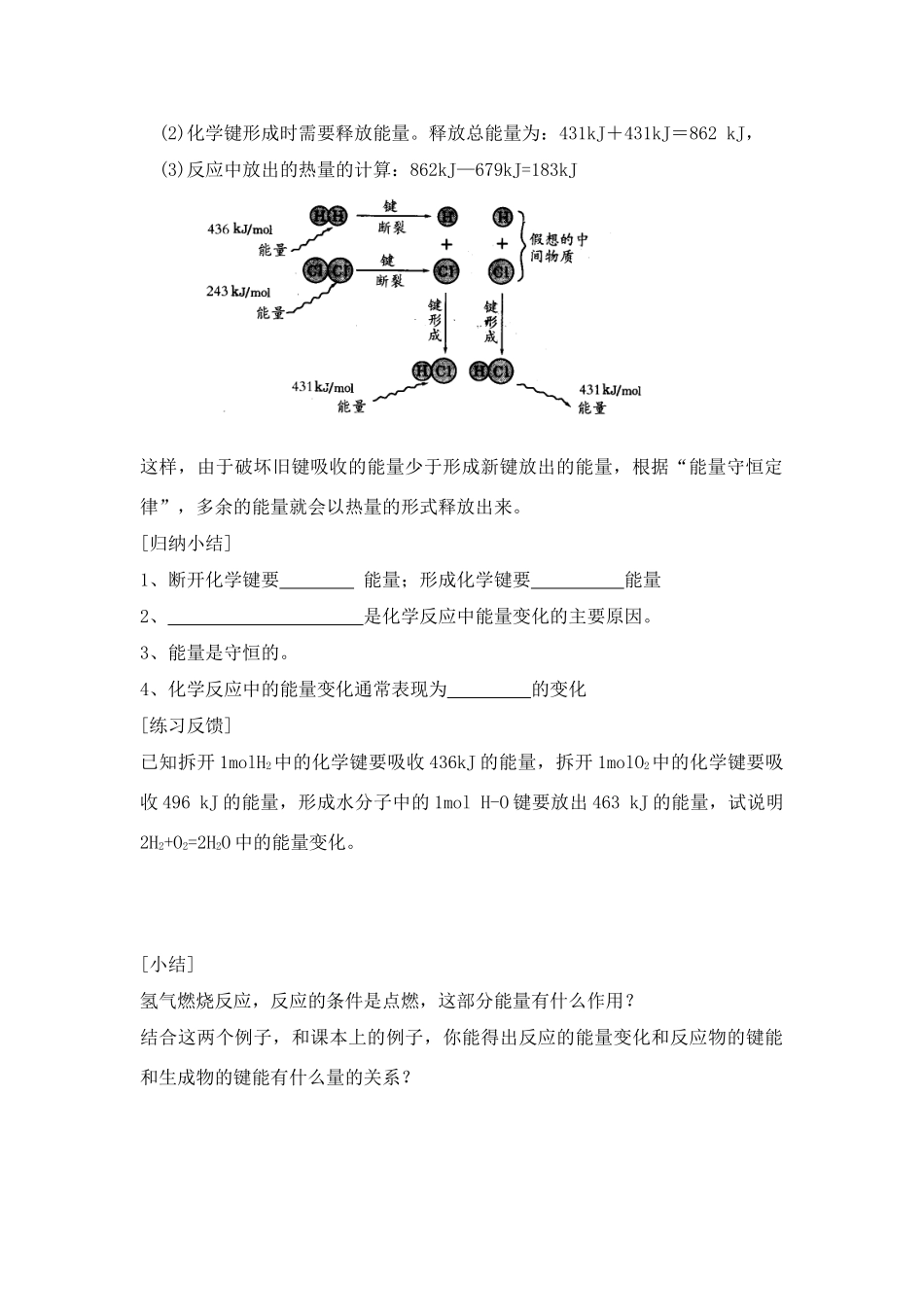
则(1)化学键断裂时需要吸收能量
吸收总能量为:436kJ+243kJ=679kJ,(2)化学键形成时需要释放能量
释放总能量为:431kJ+431kJ=862