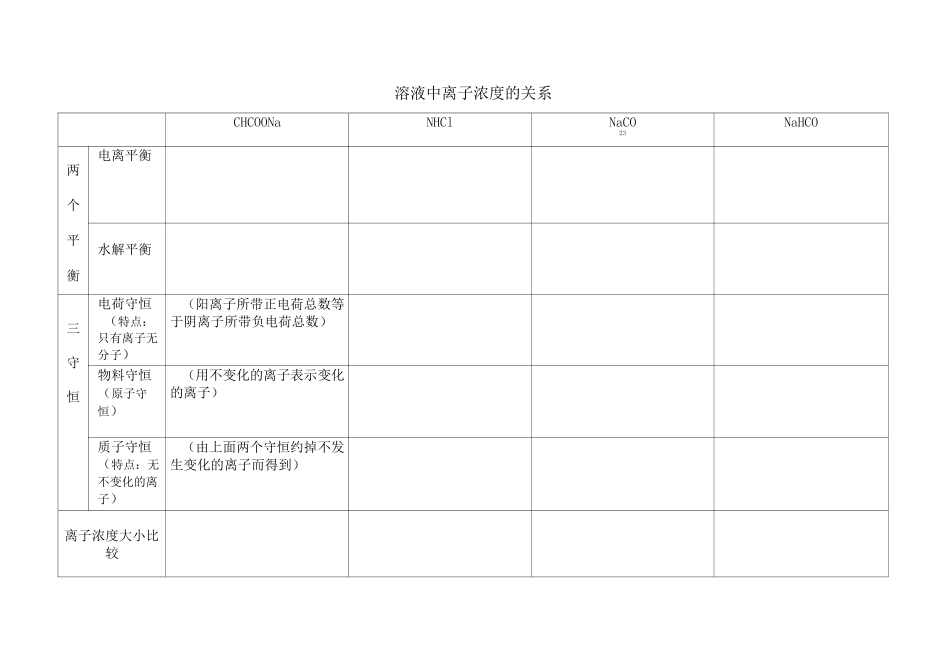
溶液中离子浓度的关系CHCOONaNHClNaCO23NaHCO两个平衡电离平衡水解平衡三守恒电荷守恒(特点:只有离子无分子)(阳离子所带正电荷总数等于阴离子所带负电荷总数)物料守恒(原子守恒)(用不变化的离子表示变化的离子)质子守恒(特点:无不变化的离子)(由上面两个守恒约掉不发生变化的离子而得到)离子浓度大小比较燮n运用三$fH”一a[看不同帑液中其他离子对该离子的罂响]・相耳不反应一7同时考虑电离和水帼T生施酸、破相互反应一离子浓度的大小比较电解质溶液中离子浓度大小比较问题,是高考的“热点”之一
多年以来全国高考化学试卷年年涉及这种题型
这种题型考查的知识点多,灵活性、综合性较强,有较好的区分度
要深入理解和熟练解决这类问题,必须弄清这类问题所涉及到的化学原理和构成这类问题的数学手段,从化学原理分析,要涉及到强弱电解质、电离平衡、水的电离、pH值、离子反应、盐类水解等基本知识;从数学手段分析,构成这类问题是,命题者常会用移项、带入具体数值、等式合并、消去某项等数学手段
这类问题涉及到的知识点主要有:一个原理、两个平衡、三个守恒、四种物质
一个原理即:化学平衡原理
两个平衡即:电离平衡和盐类的水解平衡
三个守恒即:溶液中阴、阳离子的电荷守恒、物料守恒、质子守恒
四种物质即:NH4CI、CH3COONa、Na2CO3、NaHCO3等
一、理清一条思路,掌握分析方法(1)首先必须形成正确的解题思路:一个原理;两类平衡;三种守恒
(2)要养成认真、细致、严谨的解题习惯,在形成正确解题思路的基础上学会常规分析方法,例如:关键性离子定位法、守恒判断法、微量法、终态分析法等
■越虫盐|—彳先判断巔式歯根足%电离为主还是以水丽至■T不过坛H_「*[gg]—T根据匝离儕况考虑电离或永嘲熟练掌握NH4CI、CH3COONa、Na2CO3、NaHCO3四种物质平衡、守恒及大小比较并能迁移二