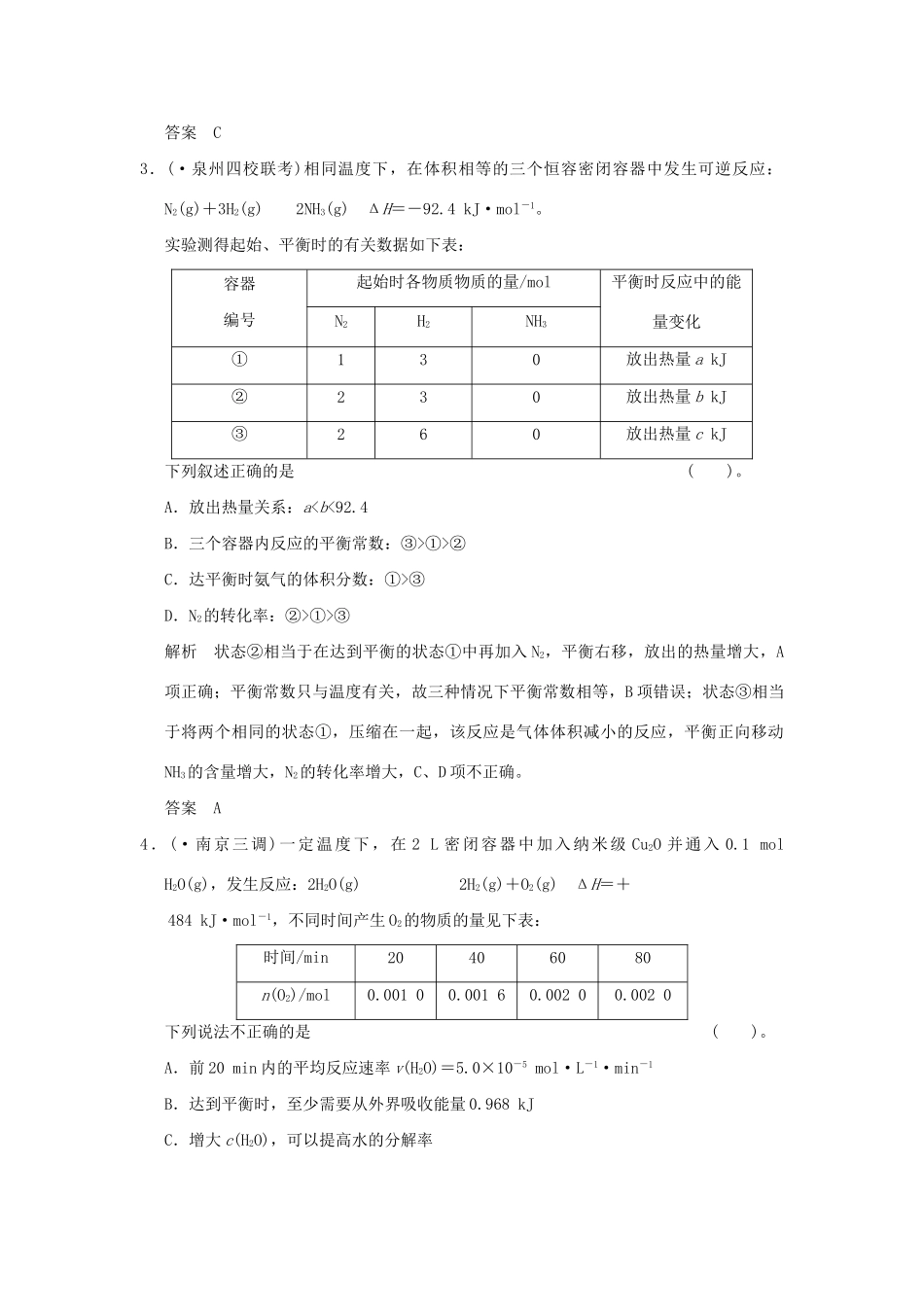
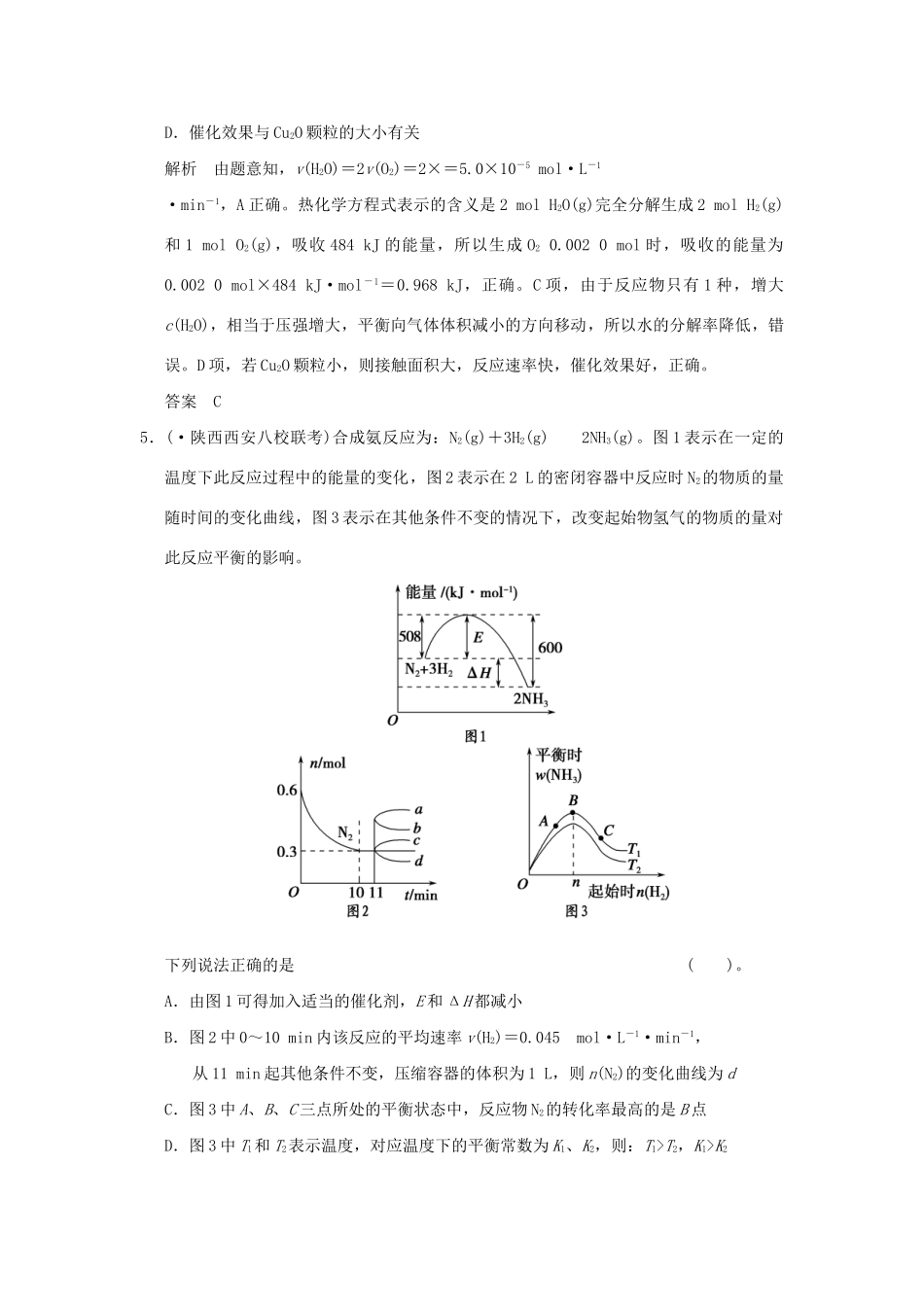
题型八化学反应速率和化学平衡的分析与判断通关演练(建议完成时间:20分钟)1.合成氨所需的氢气可用煤和水作原料经过多步反应制得,其中的一步反应为:CO(g)+H2O(g)CO2(g)+H2(g)ΔH③D.N2的转化率:②>①>③解析状态②相当于在达到平衡的状态①中再加入N2,平衡右移,放出的热量增大,A项正确;平衡常数只与温度有关,故三种情况下平衡常数相等,B项错误;状态③相当于将两个相同的状态①,压缩在一起,该反应是气体体积减小的反应,平衡正向移动NH3的含量增大,N2的转化率增大,C、D项不正确
答案A4.(·南京三调)一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0
1molH2O(g),发生反应:2H2O(g)2H2(g)+O2(g)ΔH=+484kJ·mol-1,不同时间产生O2的物质的量见下表:时间/min20406080n(O2)/mol0
0020下列说法不正确的是()
A.前20min内的平均反应速率v(H2O)=5
0×10-5mol·L-1·min-1B.达到平衡时,至少需要从外界吸收能量0
968kJC.增大c(H2O),可以提高水的分解率D.催化效果与Cu2O颗粒的大小有关解析由题意知,v(H2O)=2v(O2)=2×=5
0×10-5mol·L-1·min-1,A正确
热化学方程式表示的含义是2molH2O(g)完全分解生成2molH2(g)和1molO2(g),吸收484kJ的能量,所以生成O20
0020mol时,吸收的能量为0
0020mol×484kJ·mol-1=0
968kJ,正确
C项,由于反应物只有1种,增大c(H2O),相当于压强增大,平衡向气体体积减小的方向移动,所以水的分解率降低,错误
D项,若Cu2O颗粒小,则接触面积大,反应速率快,催化效果好,正确