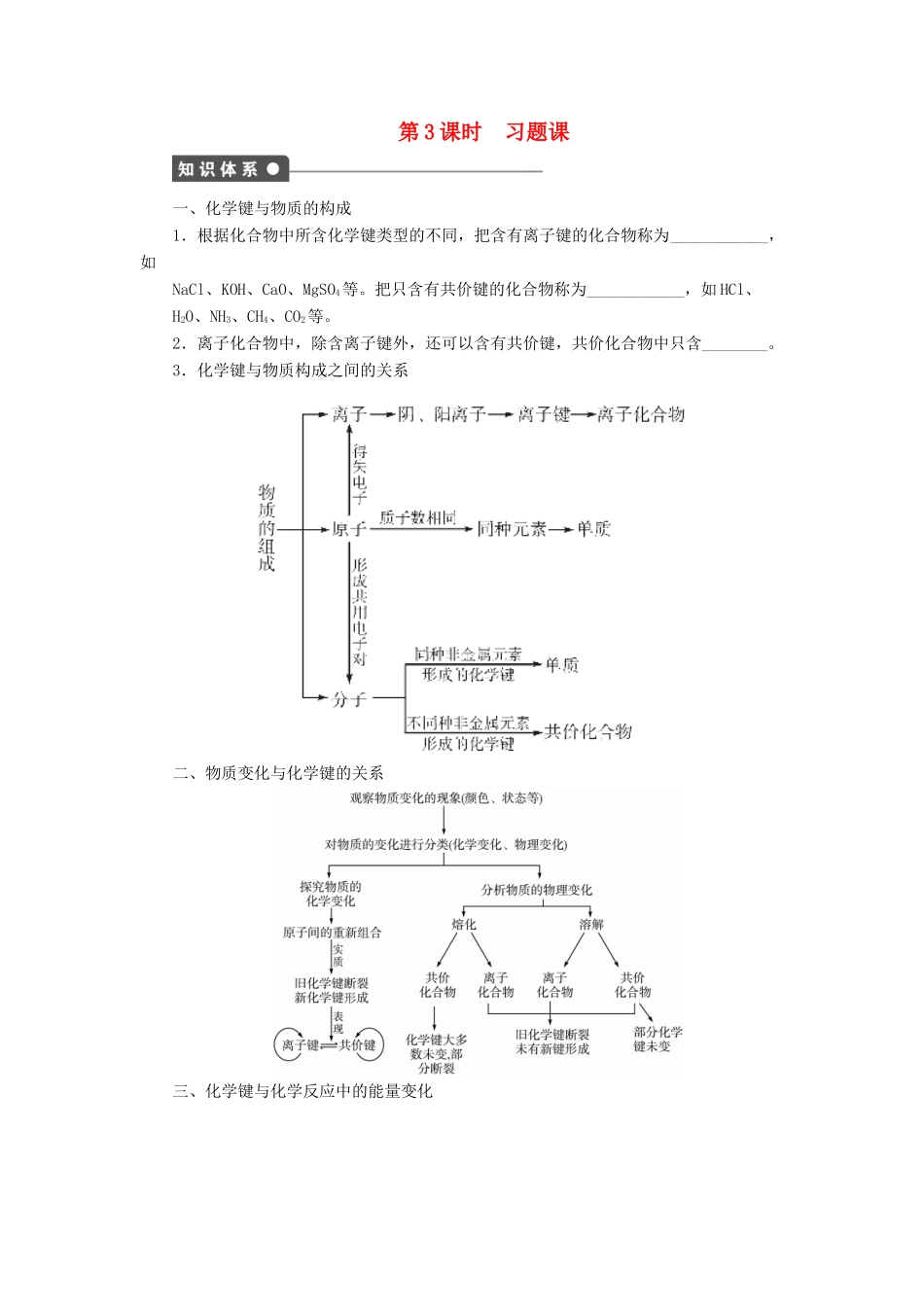
第3课时习题课一、化学键与物质的构成1.根据化合物中所含化学键类型的不同,把含有离子键的化合物称为____________,如NaCl、KOH、CaO、MgSO4等。把只含有共价键的化合物称为____________,如HCl、H2O、NH3、CH4、CO2等。2.离子化合物中,除含离子键外,还可以含有共价键,共价化合物中只含________。3.化学键与物质构成之间的关系二、物质变化与化学键的关系三、化学键与化学反应中的能量变化一、选择题(本题包括10小题)1.根据你对化学反应的实质的理解,你认为下列变化中属于化学反应的是()A.氯化钠加热熔化B.石墨在高温下转化为金刚石C.氯化氢气体溶于水D.铁被磁铁吸引2.下列说法正确的是()A.含有共价键的化合物一定是共价化合物B.单质分子中一定存在化学键C.只由非金属元素组成的化合物可以是离子化合物D.MgCl2既含离子键,又含共价键3.下列说法正确的是()A.分解反应大多数是释放能量的反应B.氢氧化钾与硝酸的反应是释放能量的反应C.燃料有足够的空气就能充分燃烧D.化学反应的过程,都可以看成是“储存”在物质内部的能量转化为热量等而被释放出来的过程4.下列分子中,所有原子的最外层均为8电子结构的是()A.H2SB.PCl3C.PCl5D.AlCl35.已知:C(金刚石)C(石墨),放出1.4kJ的热量;C(金刚石)+O2CO2(g),放出热量为Q1;C(石墨)+O2CO2(g),放出热量为Q2。根据已述反应事实,所得出的正确结论是()A.Q1=Q2B.Q2>Q1C.Q1>Q2D.金刚石比石墨稳定6.氢气在氧气中燃烧产生淡蓝色火焰,在反应中,破坏1molH—H键消耗的能量为Q1kJ,破坏1molO===O键消耗的能量为Q2kJ,形成1molH—O键释放的能量为Q3kJ。下列关系式中正确的是()A.2Q1+Q2>4Q3B.2Q1+Q2<4Q3C.Q1+Q2