定量测定实验学案备考知识实验项目包括:一定温度下硝酸钾溶解度的测定、硫酸铜晶体中结晶水含量的测定、质量百分比浓度溶液的配制、物质的量浓度溶液的配制、酸碱中和滴定、中和热测定
保证测定结果具有较高准确度和精确度对于实验结果的分析,一般是要求考生分析实验的关键、细节以及产生误差的因素等
备考练习1、某种含有少量氧化钠的过氧化钠试样(已知试样质量为1.560g、锥形瓶和水的质量190.720g),利用左图装置测定混合物中Na2O2的质量分数,每隔相同时间读得电子天平的数据如表:(1)写出Na2O2和H2O反应的化学方程式(2)计算过氧化钠质量分数时,必需的数据是不必作第6次读数的原因是(3)测定上述样品(1.560g)中Na2O2质量分数的另一种方案,其操作流程如下:①操作Ⅱ的名称是②需直接测定的物理量是③测定过程中需要的仪器有电子天平、蒸发皿、酒精灯,还需要、(固定、夹持仪器除外)④在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果(填偏大、偏小或不变)
2、甲醛是世界卫生组织(WHO)确认的致癌物和致畸物质之一
我国规定:室内甲醛含量不得超过0
08mg·m-3
某研究性学习小组欲利用酸性KMnO4溶液测定空气中甲醛的含量,请你参与并协助他们完成相关学习任务
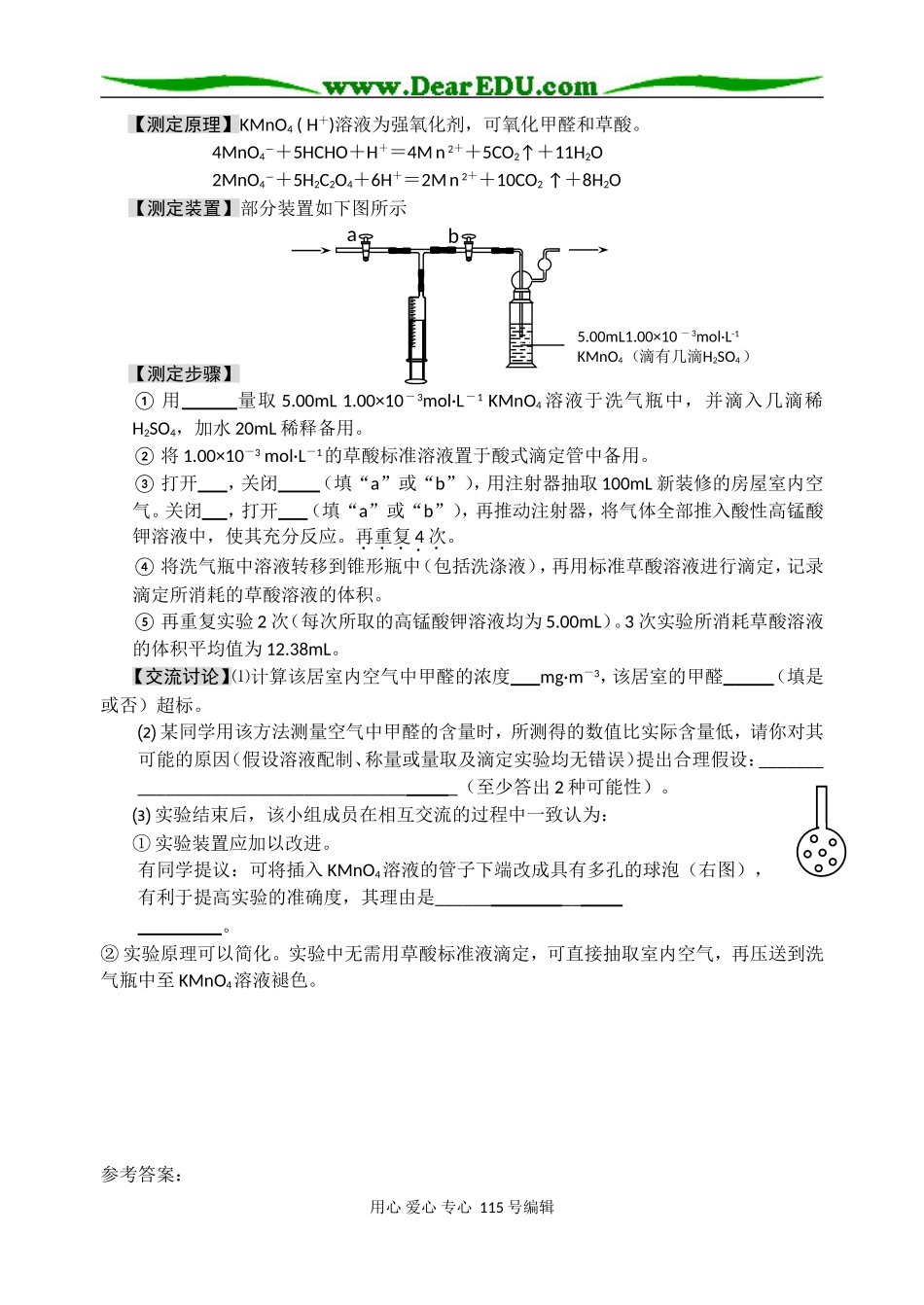
用心爱心专心115号编辑【测定原理】KMnO4(H+)溶液为强氧化剂,可氧化甲醛和草酸
4MnO4―+5HCHO+H+=4Mn2++5CO2↑+11H2O2MnO4―+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O【测定装置】部分装置如下图所示【测定步骤】①用量取5
00×10-3mol·L-1KMnO4溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用
00×10-3mol·L-1的草酸标准溶液置于酸式滴定管中备用
③打开,关闭(填“a”或“b”),用注射器抽取10