第2课时元素周期律一、元素原子结构的周期性变化1.元素原子核外电子排布的周期性变化周期序数原子序数电子层数最外层电子数一1~211―→2二3~1021―→8三11~1831―→8结论:随着原子序数的递增,元素原子的最外层电子排布呈现____________的周期性变化(H、He除外)2
元素原子半径的周期性变化周期序数原子序数原子半径的变化二3~9逐渐____三11~17逐渐____结论:随着原子序数的递增,元素原子半径呈现________的周期性变化3
微粒半径大小比较的方法(1)电子层数相同(即同周期)时,随原子序数的递增,原子半径逐渐________
(2)最外层电子数相同(即同主族)时,随电子层数(原子序数)的递增,原子半径逐渐________
(3)电子层结构相同的不同离子,原子序数越大,离子半径____
二、元素性质的周期性变化1.元素化合价的周期性变化周期序数原子序数化合价(最高价、最低价)的变化一1~2+1―→0二3~10最高正价:__________最低负价:__________三11~18最高正价:__________最低负价:__________结论:随着原子序数的递增,元素的最高正价呈现________、最低负价呈现__________的周期性变化主族元素化合价变化规律与原子结构的关系元素的最高正价数值上等于该元素原子的最外层________,随元素原子序数的递增,最外层电子数增多,最高化合价的数值______;最低负价的绝对值与最外层电子数之和等于____,随最外层电子数的增加,最低负价的绝对值______
第二周期的氧元素和氟元素只有负价没有正价
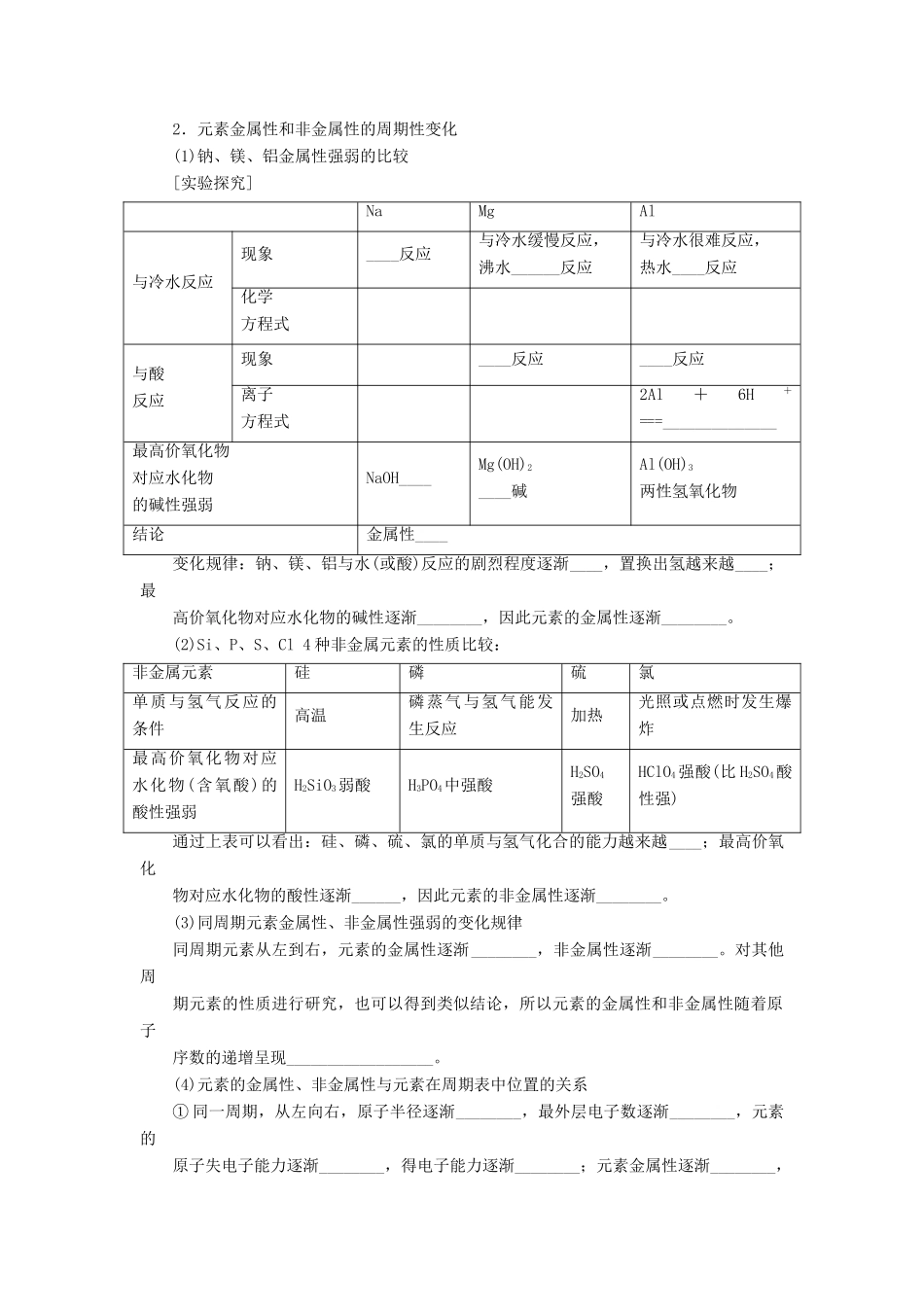
2.元素金属性和非金属性的周期性变化(1)钠、镁、铝金属性强弱的比较[实验探究]NaMgAl与冷水反应现象____反应与冷水缓慢反应,沸水______反应与冷水很难反应,热水____反应化学方程式与酸反