第3讲铁及其化合物[考纲要求]1
了解铁及其重要化合物的主要性质及其应用
以Fe2+、Fe3+的相互转化为例,理解变价金属元素的氧化还原反应
能鉴别溶液中的Fe2+、Fe3+
考点一用物质分类思想认识铁及其重要化合物1.铁的存在2.铁的性质(1)物理性质纯铁具有金属的共性,如具有银白色金属光泽和良好的延展性,是电和热的良导体,具有能被磁铁吸引的特性,纯铁有很强的抗腐蚀能力
(2)化学性质:铁是较活泼的金属,发生化学反应时可生成+2、+3两种价态的化合物
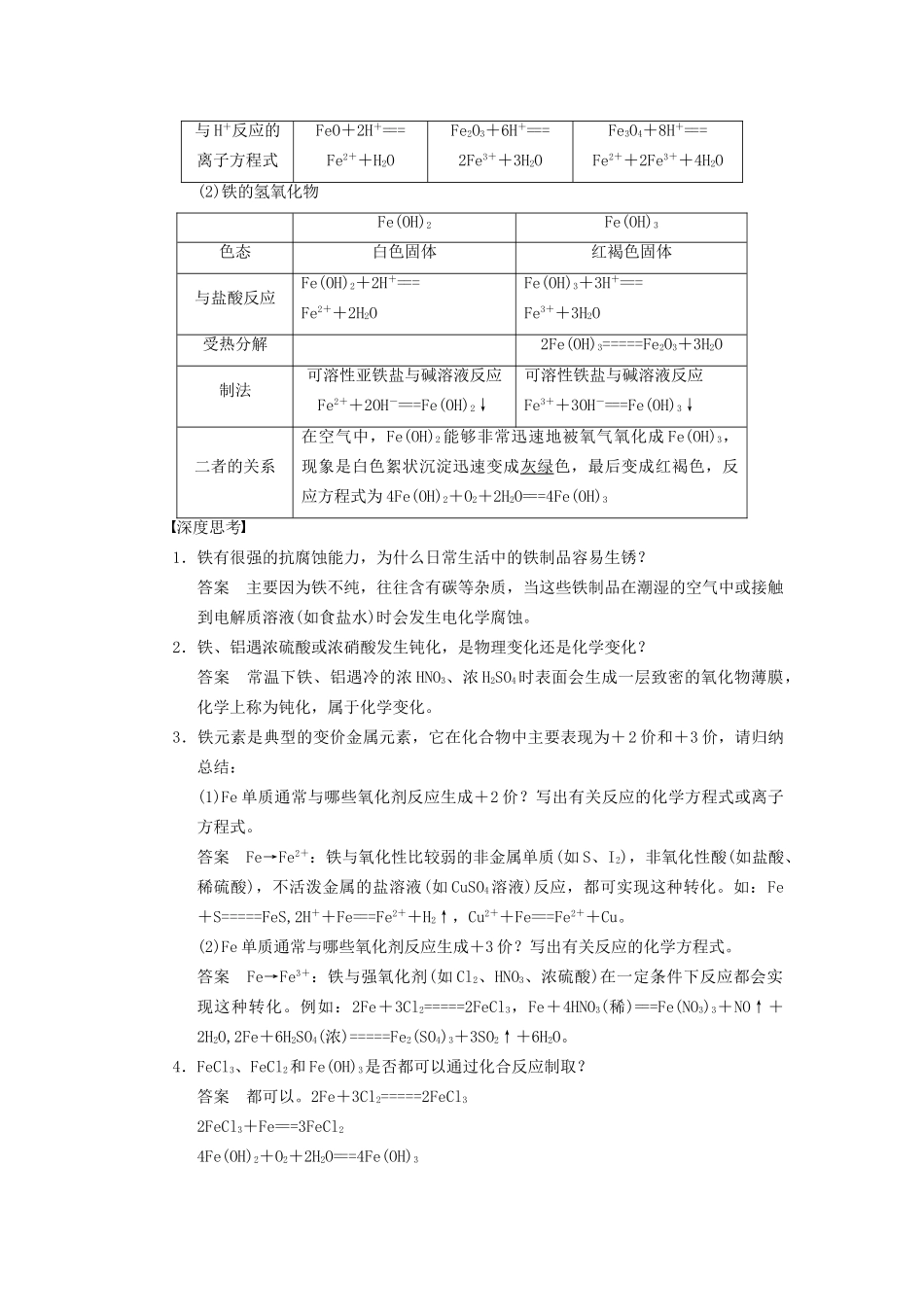
用化学方程式或离子方程式表示下列变化Fe+Fe+H2O(g)――→④3Fe+4H2O(g)=====Fe3O4+4H2Fe—3.铁的氧化物和氢氧化物(1)铁的氧化物化学式FeOFe2O3Fe3O4俗名铁红磁性氧化铁颜色状态黑色粉末红棕色粉末黑色晶体(有磁性)溶解性难溶于水难溶于水难溶于水铁的化合价+2+3+2,+3稳定性不稳定稳定稳定与H+反应的离子方程式FeO+2H+===Fe2++H2OFe2O3+6H+===2Fe3++3H2OFe3O4+8H+===Fe2++2Fe3++4H2O(2)铁的氢氧化物Fe(OH)2Fe(OH)3色态白色固体红褐色固体与盐酸反应Fe(OH)2+2H+===Fe2++2H2OFe(OH)3+3H+===Fe3++3H2O受热分解2Fe(OH)3=====Fe2O3+3H2O制法可溶性亚铁盐与碱溶液反应Fe2++2OH-===Fe(OH)2↓可溶性铁盐与碱溶液反应Fe3++3OH-===Fe(OH)3↓二者的关系在空气中,Fe(OH)2能够非常迅速地被氧气氧化成Fe(OH)3,现象是白色絮状沉淀迅速变成灰绿色,最后变成红褐色,反应方程式为4Fe(OH)2+O2+2H2O===4Fe(OH)3深度思考1.铁有很强的抗腐蚀能力,为什么日常生活中的铁制品容易生锈
答案主要因为铁不纯,往往含有