第4讲物质的量浓度及其溶液的配制[考纲要求]1
了解溶解度、饱和溶液的概念
了解物质的量浓度的含义
能按要求配制一定物质的量浓度的溶液,会进行有关误差分析
会根据物质的量与溶液的体积、溶液的物质的量浓度之间的相互关系进行有关计算
考点一物质的量浓度及相关计算物质的量浓度与溶质质量分数的比较内容物质的量浓度质量分数定义以单位体积溶液里含有多少摩尔溶质来表示溶液组成的物理量用溶质质量与溶液质量之比来表示溶液组成的物理量溶质的单位molg溶液的单位Lg计算公式c=w=×100%特别提醒这里V是溶液的体积,它不是溶剂的体积,也不是溶剂和溶质的体积之和
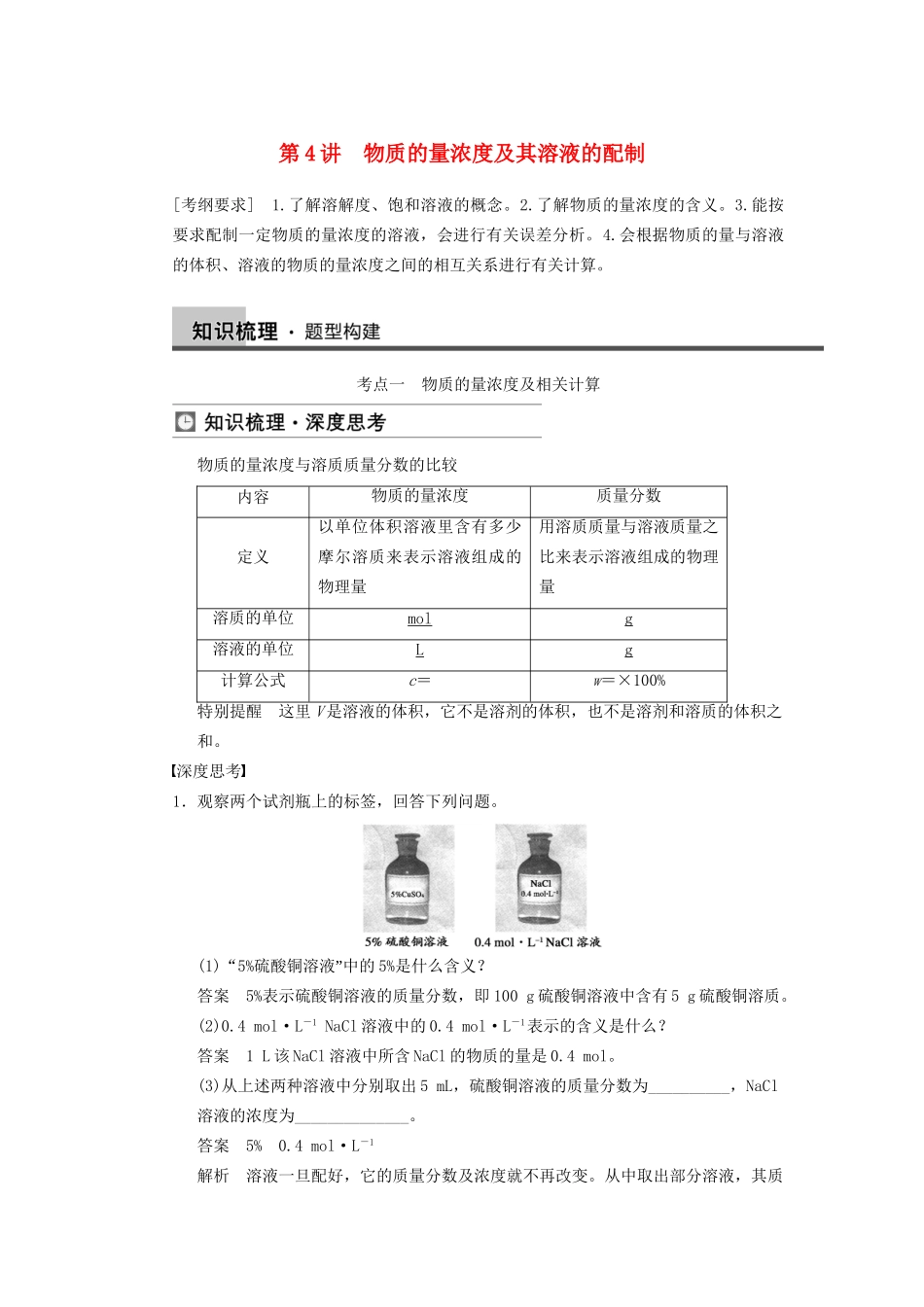
深度思考1.观察两个试剂瓶上的标签,回答下列问题
(1)“5%”硫酸铜溶液中的5%是什么含义
答案5%表示硫酸铜溶液的质量分数,即100g硫酸铜溶液中含有5g硫酸铜溶质
4mol·L-1NaCl溶液中的0
4mol·L-1表示的含义是什么
答案1L该NaCl溶液中所含NaCl的物质的量是0
(3)从上述两种溶液中分别取出5mL,硫酸铜溶液的质量分数为__________,NaCl溶液的浓度为______________
4mol·L-1解析溶液一旦配好,它的质量分数及浓度就不再改变
从中取出部分溶液,其质量分数及浓度也不变
2.填空(1)将Na通入水中,其溶质是__________;(2)将Na2O溶于水,其溶质是__________;(3)将CuSO4·5H2O溶于水中,其溶质是__________;(4)将SO3溶于水,其溶质是________
答案(1)NaOH(2)NaOH(3)CuSO4(4)H2SO4题组一根据cB=的计算1.将10
6gNa2CO3溶于水配成1L溶液(1)该溶液中Na2CO3的物质的量浓度为__________,溶液中Na+的物质的量浓度为__________