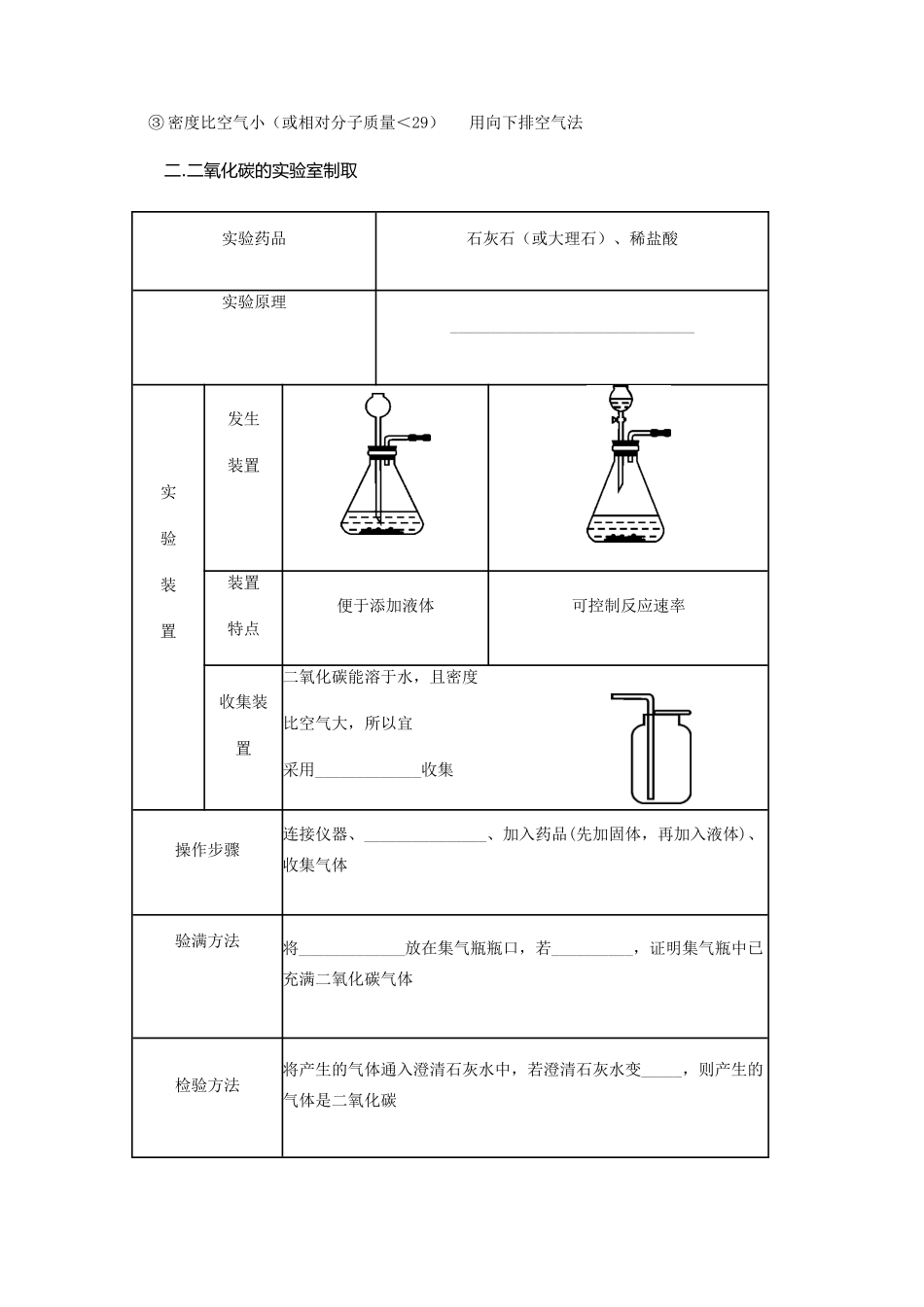
第六单元碳和碳的氧化物【考点知识梳理】考点一碳的单质【考点解读】1.常见碳单质的物理性质及用途2.碳单质的化学性质。3.还原反应一.常见碳单质的物理性质及用途碳单质性质用途金刚石无色透明、正八面体的固体,天然存在_____的物质裁玻璃、切割大理石、加工坚硬的金属、钻探机的钻头石墨质软、有滑腻感、具有优良的______制铅笔芯、石墨电刷、石墨电极、润滑剂C60C60是由_______构成的,1个C60分子由__________构成,以单质形式存在的碳,形似足球可能广泛应用于超导、催化、材料、医学及生物等领域性质差异的原因______________________不同,导致几种碳单质的物理性质有很大差异,但化学性质仍相似二.无定形碳:1.由石墨的微小晶体和少量杂质构成.主要有:焦炭,木炭,活性炭,炭黑等.2、活性炭、木炭具有强烈的____________(因为具有疏松多孔的结构),木炭可用于食品、工业产品中除去色素、异味等,活性炭可用于___________中除去毒气、制糖业中脱色以制白糖;焦炭用于冶铁,炭黑加到橡胶里能够增加轮胎的耐磨性。注意:吸附性是活性炭、木炭的_____________性质。(活性炭的吸附性能更好)三.单质碳的化学性质稳定性常温下,碳的化学性质不活泼,所以古代字画能够保存很长时间而不变色可燃性①燃烧充分时:C+O2点燃CO2;②燃烧不充分时:_______________。说明了相同反应物在不同条件下反应产物可能不同(相同点是均放出热)还原性①与CuO反应:________________________;②与Fe2O3反应:_____________________________;(焦炭可以把铁从它的氧化物矿石里还原出来)③与CO2反应:_________________考点二二氧化碳制取的研究【考点解读】1、制取气体的一般设计思路和方法2、二氧化碳的实验室制法:包括药品、反应原理、实验装置、操作步骤、收集方法、检验方法及验满方法。一、实验室制取气体的思路:1发生装置:由___________及__________决定:①反应物是固体,需加热,制气体时则用高锰酸钾制O2的发生装置。②反应物是固体与液体,不需要加热,制气体时则用制CO2的发生装置。2收集装置:由气体的_______及___________(有时还要考虑气体是否有毒,污染空气)决定:①难溶于水且不与水反应用排水法收集CO只能用排水法②密度比空气大(或相对分子质量>29)用向上排空气法CO2只能用向上排空气法③密度比空气小(或相对分子质量<29)用向下排空气法二.二氧化碳的实验室制取实验药品石灰石(或大理石)、稀盐酸实验原理______________________________实验装置发生装置装置特点便于添加液体可控制反应速率收集装置二氧化碳能溶于水,且密度比空气大,所以宜采用_____________收集操作步骤连接仪器、_______________、加入药品(先加固体,再加入液体)、收集气体验满方法将_____________放在集气瓶瓶口,若__________,证明集气瓶中已充满二氧化碳气体检验方法将产生的气体通入澄清石灰水中,若澄清石灰水变_____,则产生的气体是二氧化碳CO2的吸收实验室常用氢氧化钠溶液来吸收二氧化碳,吸收时导管应插入液面以___,其发生反应的化学方程式为______________________________【特别提醒】1.药品的选择(1)反应物一般不选浓盐酸和稀硫酸,原因是浓盐酸易挥发出氯化氢气体,使制得的二氧化碳不纯;而稀硫酸与大理石反应生成的硫酸钙微溶,附着在大理石表面,阻止反应的进一步发生;(2)反应一般不选用碳酸钠粉末,这是由于碳酸钠粉末与稀盐酸接触面积大,反应速率过快,不便于收集气体。2.实验操作(1)使用长颈漏斗时必须插到液面以下,否则生成的气体会从长颈漏斗口溢出;(2)反应容器中的导管不要伸入太长,更不能插入液面以下,否则气体无法排出;(3)收集装置中的导管应伸入集气瓶底部,否则不利于空气的排出;(4)用氢氧化钠溶液吸收二氧化碳时,导管应插到液面以下。三、二氧化碳的工业制法:1、煅烧石灰石:_____________________________________(分解反应)2、联系:明代于谦《石灰吟》诗句所蕴含的变化(在后面三句写出化学方程式):千锤万凿出深山(物理变化),烈火焚烧若等闲粉身碎骨浑不怕要留清白在人间考点三二氧化碳和一氧化碳【考点解读】1.知道二氧化碳和一...