化学反应速率和化学平衡1.下列反应不是可逆反应的是()A.CO2+H2O=H2CO3和H2CO3=CO2+H2OB.2H2O2H2↑+O2↑和2H2+O2点燃2H2OC.2SO2+O22SO3和2SO32SO2+O2D.H2+I2△2HI和2HI△H2+I22.用于净化汽车尾气的反应:2NO(g)+2CO(g)2CO2(g)+N2(g),已知该反应速率极慢,570K时平衡常数为1×1059
下列说法正确的是()A.装有尾气净化装置的汽车排出的气体中不再含有NO或COB.提高尾气净化效率的常用方法是升高温度C.提高尾气净化效率的最佳途径是研制高效催化剂D.570K时该反应正向进行的程度很大,故使用催化剂并无实际意义3.500℃条件下,在恒容密闭容器中,充入1molNO2存在如下平衡2NO2(g)N2O4(g),平衡后,向容器内再充入1molNO2,下列说法正确的()A.容器内气体颜色先变深后变浅,最后比原来还要浅B.反应向正反应方向移动C.NO2的转化率变小D.N2O4的体积分数一定增大4.设v(正)和v(逆)分别表示可逆反应的正反应速率和逆反应速率
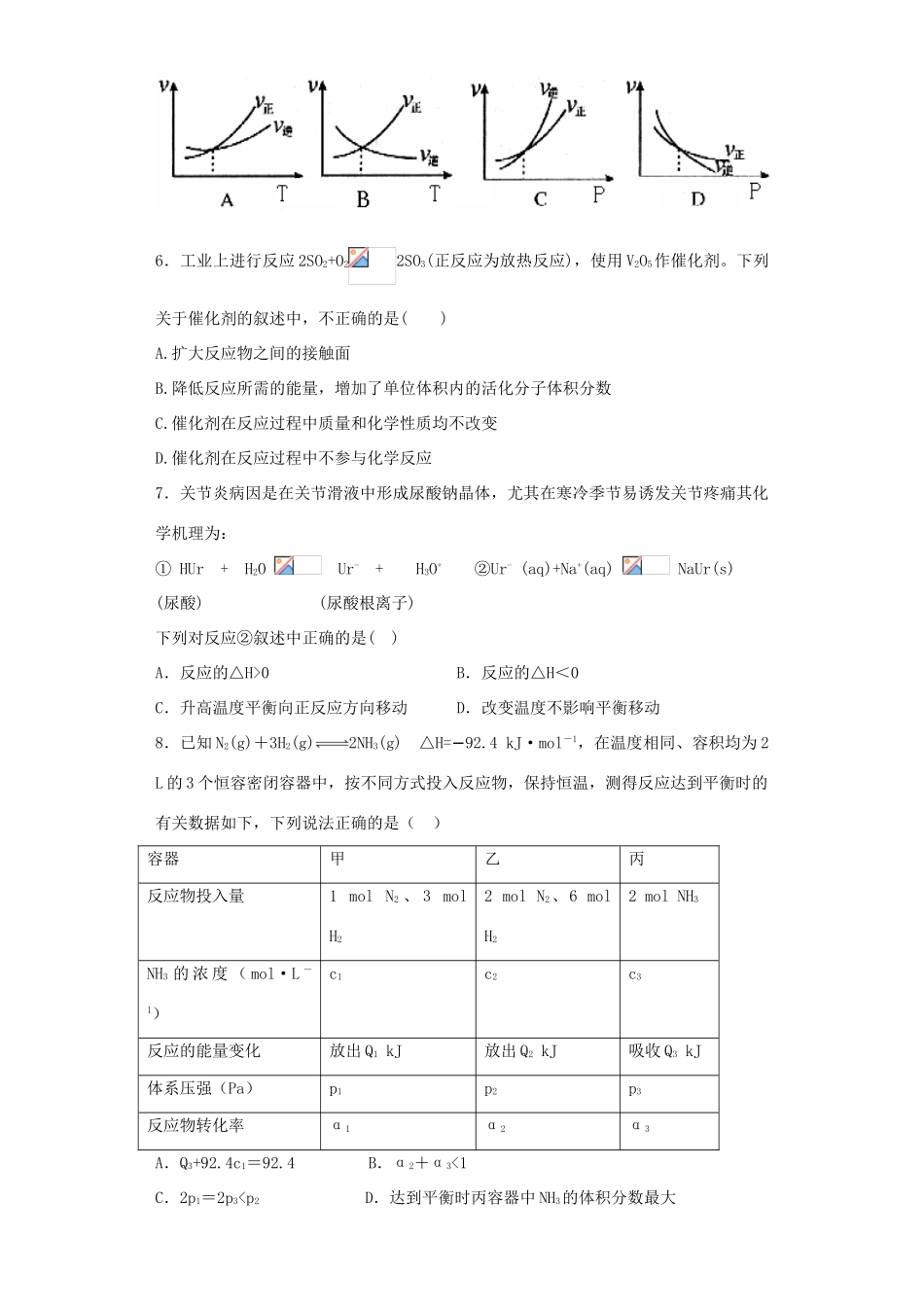
在一定温度下可逆反应N2+3H2V2O5△高温、高压催化剂浓硫酸Δ180℃催化剂充电放电催化剂Δ放电充电2NH3达到平衡时()A.V(逆)>V(正)B.V(逆)V(正),正逆反应停止D.V(逆)=V(正),正逆反应仍进行5.下列各图是温度T(或压强P)对f反应2A(s)+2B(g)2C(g)+D(g)△H>0的正、逆反应速率的影响,曲线交点表示建立平衡时的温度或压强,其中正确的是()6.工业上进行反应2SO2+O22SO3(正反应为放热反应),使用V2O5作催化剂
下列关于催化剂的叙述中,不正确的是()A
扩大反应物之间的接触面B
降低反应所需的能量,增加了单位体积内的活化分子体积分数C
催化剂在反应过程中质量和化学性质均不改变