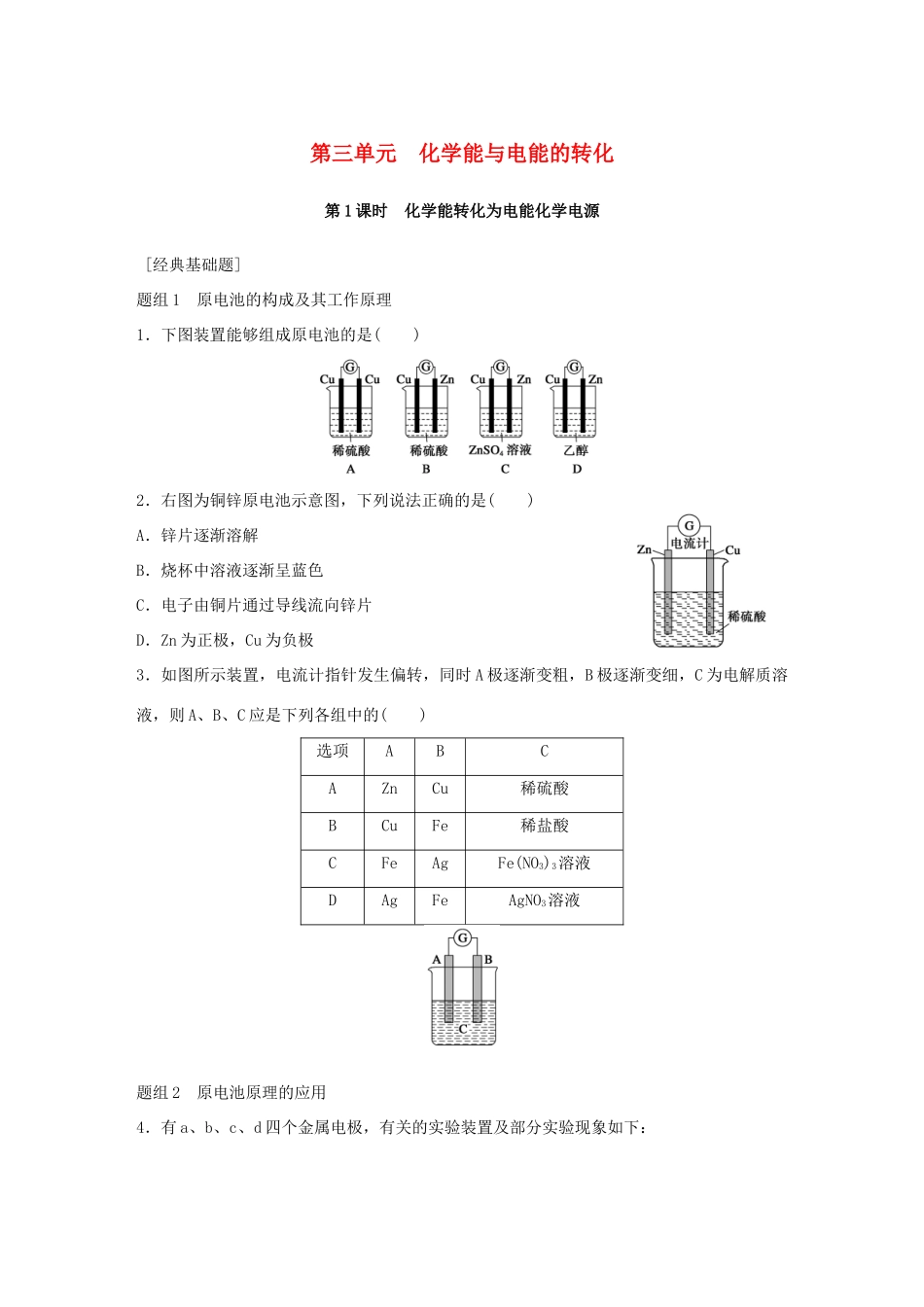
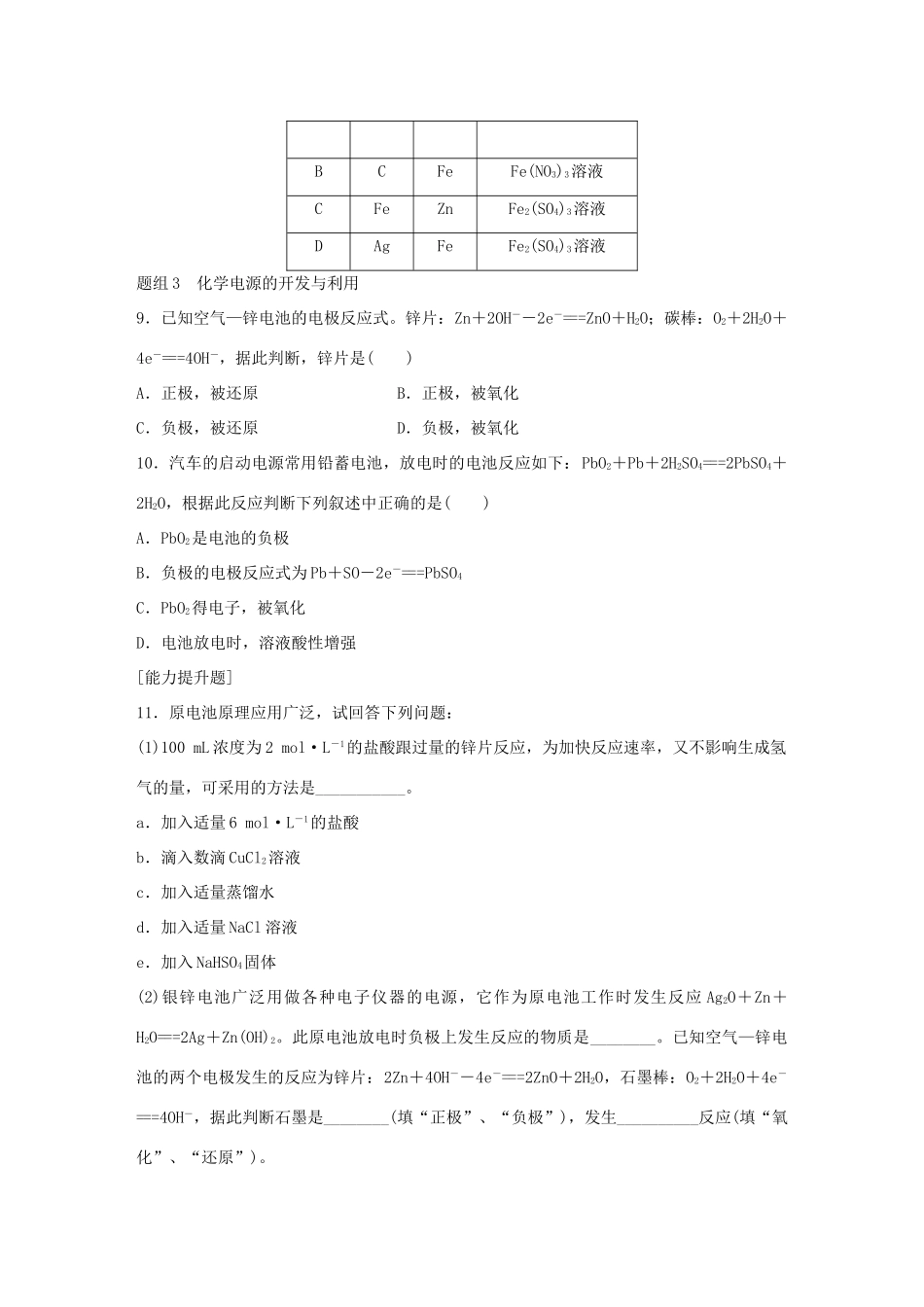
第三单元化学能与电能的转化第1课时化学能转化为电能化学电源[经典基础题]题组1原电池的构成及其工作原理1.下图装置能够组成原电池的是()2.右图为铜锌原电池示意图,下列说法正确的是()A.锌片逐渐溶解B.烧杯中溶液逐渐呈蓝色C.电子由铜片通过导线流向锌片D.Zn为正极,Cu为负极3.如图所示装置,电流计指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的()选项ABCAZnCu稀硫酸BCuFe稀盐酸CFeAgFe(NO3)3溶液DAgFeAgNO3溶液题组2原电池原理的应用4.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:实验装置部分实验现象a极质量减小,b极质量增大生,c极无变化有气体产生极由此可判断这四种金属的活动性顺序是()A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c5.某原电池反应的离子方程式为Fe+2H+===Fe2++H2↑,则下列说法正确的是()A.HNO3为电解质溶液B.锌为原电池正极C.铁极质量不变D.铜为原电池正极6.钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为2Fe+2H2O+O2===2Fe2++4OH-。以下说法正确的是()A.负极发生的反应为Fe-2e-===Fe2+B.正极发生的反应为2H2O+O2+2e-===4OH-C.钢铁被腐蚀最后生成的铁锈为Fe(OH)2D.钢柱在水下部分比在空气与水交界处更容易腐蚀7.钢铁生锈过程发生如下反应:①2Fe+O2+2H2O===2Fe(OH)2;②4Fe(OH)2+O2+2H2O===4Fe(OH)3;③2Fe(OH)3===Fe2O3+3H2O。下列说法正确的是()A.反应①、②中电子转移数目相等B.反应①中氧化剂是氧气和水C.与铜质水龙头连接的钢质水管不易发生腐蚀D.钢铁在潮湿的空气中不能发生电化学腐蚀8.某原电池的总反应的离子方程式为2Fe3++Fe===3Fe2+,不能实现该反应的原电池是()选项正极负极电解质溶液ACuFeFeCl3溶液BCFeFe(NO3)3溶液CFeZnFe2(SO4)3溶液DAgFeFe2(SO4)3溶液题组3化学电源的开发与利用9.已知空气—锌电池的电极反应式。锌片:Zn+2OH--2e-===ZnO+H2O;碳棒:O2+2H2O+4e-===4OH-,据此判断,锌片是()A.正极,被还原B.正极,被氧化C.负极,被还原D.负极,被氧化10.汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4===2PbSO4+2H2O,根据此反应判断下列叙述中正确的是()A.PbO2是电池的负极B.负极的电极反应式为Pb+SO-2e-===PbSO4C.PbO2得电子,被氧化D.电池放电时,溶液酸性增强[能力提升题]11.原电池原理应用广泛,试回答下列问题:(1)100mL浓度为2mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的量,可采用的方法是___________。a.加入适量6mol·L-1的盐酸b.滴入数滴CuCl2溶液c.加入适量蒸馏水d.加入适量NaCl溶液e.加入NaHSO4固体(2)银锌电池广泛用做各种电子仪器的电源,它作为原电池工作时发生反应Ag2O+Zn+H2O===2Ag+Zn(OH)2。此原电池放电时负极上发生反应的物质是________。已知空气—锌电池的两个电极发生的反应为锌片:2Zn+4OH--4e-===2ZnO+2H2O,石墨棒:O2+2H2O+4e-===4OH-,据此判断石墨是________(填“正极”、“负极”),发生__________反应(填“氧化”、“还原”)。(3)根据原电池原理可设计成化学电源,下列关于原电池的说法不正确的是__________________。a.手机上用的锂离子电池属于二次电池b.甲醇燃料电池可将化学能转化为电能c.锌锰干电池中,锌电极为负极d.所有释放能量的反应都能通过原电池实现(4)目前已经使用的氢氧燃料电池的基本反应是X极:O2+2H2O+4e-===4OH-,Y极:H2+2OH--2e-===2H2O。①X是________极,发生________反应(填“氧化”或“还原”),总反应方程式为______________________。②若反应后得到5.4g液态水,此时氢氧燃料电池转移的电子数为__________。12.市场上出售的“热敷袋”,其主要成分是铁屑、碳粉、木屑和少量氯化钠、水等。热敷袋启用之前用塑料袋密封与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完毕后,会发现有大量铁锈存在。据此回答:(1)热敷袋使用时,放出热量的原因是________________________________________________________________________。(2)碳粉的主要...