化学实验(B)一、选择题(本题包括10小题,每小题5分,共50分)1
用铁制备较纯净的三氧化二铁,下列实验方案最好的是A.使铁在潮湿的空气中缓慢氧化B.铁在氯气中燃烧,加水溶解,加入足量NaOH溶液,过滤、洗涤、然后充分加热分解C.使铁溶解于稀硫酸,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解D.使铁与足量稀硝酸反应,然后加入足量NaOH溶液,过滤、洗涤,然后充分加热分解2
下列说法正确的是A.仅用AgNO3溶液便可鉴别亚硝酸钠和食盐B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大C.乙酸与乙醇的混合液可用分液漏斗进行分离D.用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低3
某氯碱厂利用废铁皮制取净水剂FeCl3溶液,最合理的生产途径是A.Cl2――→FeCl3――→FeCl3溶液B.Cl2――→HCl――→盐酸――→FeCl2溶液――→FeCl3C.Cl2――→HCl――→盐酸――→FeCl2溶液――→FeCl3溶液D
FeCl3溶液4
下列实验设计能够成功的是A.检验亚硫酸钠试样是否变质:试样――→溶液――――→白色沉淀――→沉淀不溶解B.除去乙酸乙酯中混有的乙酸:混合液――――――――――→溶液分层――→得上层液体C.证明酸性条件下H2O2氧化性比I2强:NaI溶液―――――――――――――――→溶液变蓝色D.鉴定盐A的成分是FeBr2:5
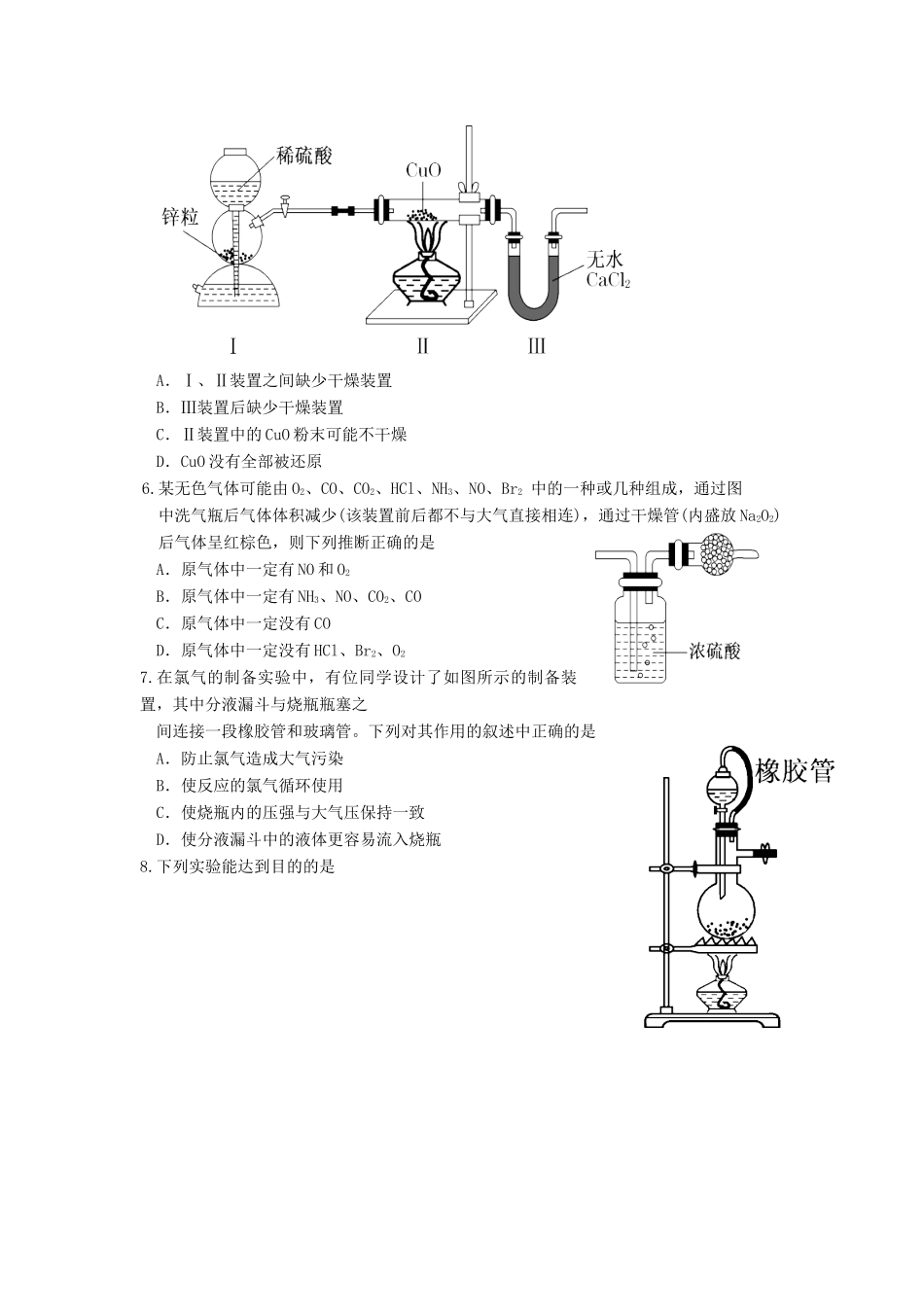
用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差
李松同学通过实验得出的结论是m(H)∶m(O)>1∶8
下列对导致这一结果原因的分析中,一定不合理的是A.Ⅰ、Ⅱ装置之间缺少干燥装置B.Ⅲ装置后缺少干燥装置C.Ⅱ装置中的CuO粉末可能不干燥D.CuO没有全部被还原6
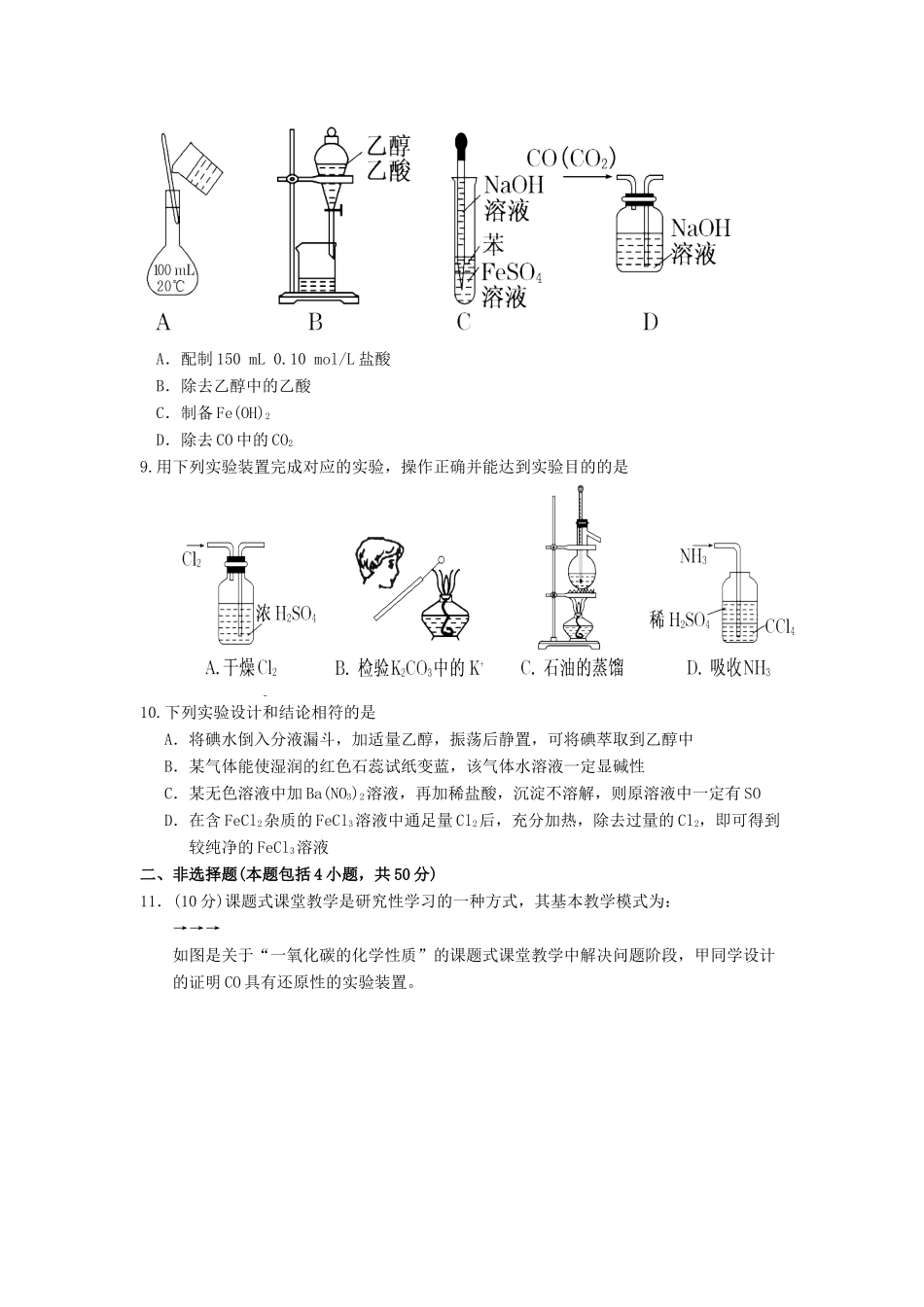
某无色气体可能由O2、CO、CO2、HCl、NH3、NO、Br2中的