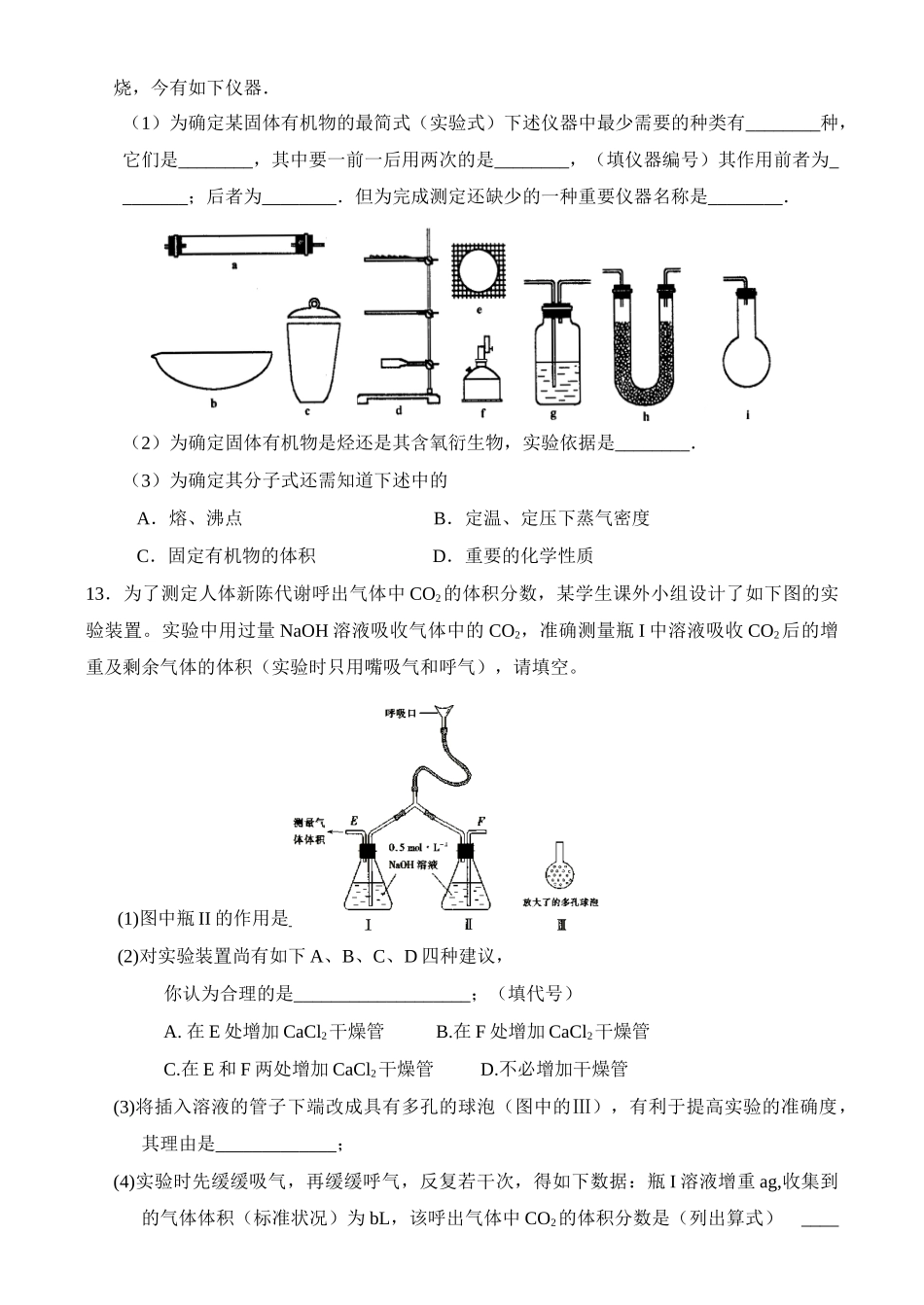
考点57定量实验与数据处理1
下列仪器“O”刻度位置正确的是()A
量筒的上端B
在滴定管上端C
在托盘天平刻度尺的正中D
在托盘天平刻度尺的右边2
准确量取25
00mL高锰酸钾溶液,可选用的仪器是()A.50mL量筒B.10mL量筒C.50mL酸式滴定管D.50mL碱式滴定管3
用某种仪器量取液体体积时,平视时读数为nmL,仰视时读数为xmL,俯视时读数为ymL,若x>n>y,则所用的仪器可能为()A.量筒B.容量瓶C.滴定管D.以上均不对4
有①、②、③三瓶体积相等,浓度都是1mol·L-1的HCl溶液,将①加热蒸发至体积减少一半,在②中加入少量CH3COONa固体(加入后溶液仍呈强酸性),③不作改变,然后以酚酞作指示剂,用NaOH溶液滴定上述三种溶液,所消耗的NaOH溶液体积是()A
③=①>②B
>>③②①C
=>③②①D
==①②③5.实验室需用480mL0
1mol·L—1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是()A.称取7
68g硫酸铜,加入500mL水B.称取12
0g胆矾配成500mL溶液C.称取8
0g硫酸铜,加入500mL水D.称取12
5g胆矾配成500mL溶液6.用质量分数为37%、密度为1
19g·mL-1的浓盐酸配制1
0mol·L-1的稀盐酸100mL
配制过程中要用到的仪器及其使用先后顺序排列正确的是()①酸式滴定管②碱式滴定管③50mL烧杯④托盘天平⑤100mL容量瓶⑥胶头滴管⑦玻璃棒A
④③⑦⑤⑥C
①③⑦⑤⑥D
①③⑤⑥⑦7
用已知浓度的盐酸滴定未知浓度的NaOH溶液时,可能有如下操作:①将标准盐酸注入酸式滴定管②锥形瓶用待测的NaOH溶液润洗③边滴边振荡锥形瓶④用标准盐酸润洗酸式滴定管⑤移取NaOH溶液,注入锥形瓶⑥往锥形瓶里溶液中滴加2滴酚酞试液⑦调整酸式滴定管内液面⑧滴定至终点
以上操作正确