第2课时元素周期表1
了解元素周期表的编排规则及结构特点
能描述元素在元素周期表中的位置
3.理解原子结构与元素在周期表中的位置的关系
元素周期表的结构[学生用书P9]1.元素周期表中的常用信息(1)元素周期表方格中的信息(2)元素周期表中金属元素与非金属元素的分区分界线附近元素的性质:既能表现出一定的金属性,又能表现出一定的非金属性
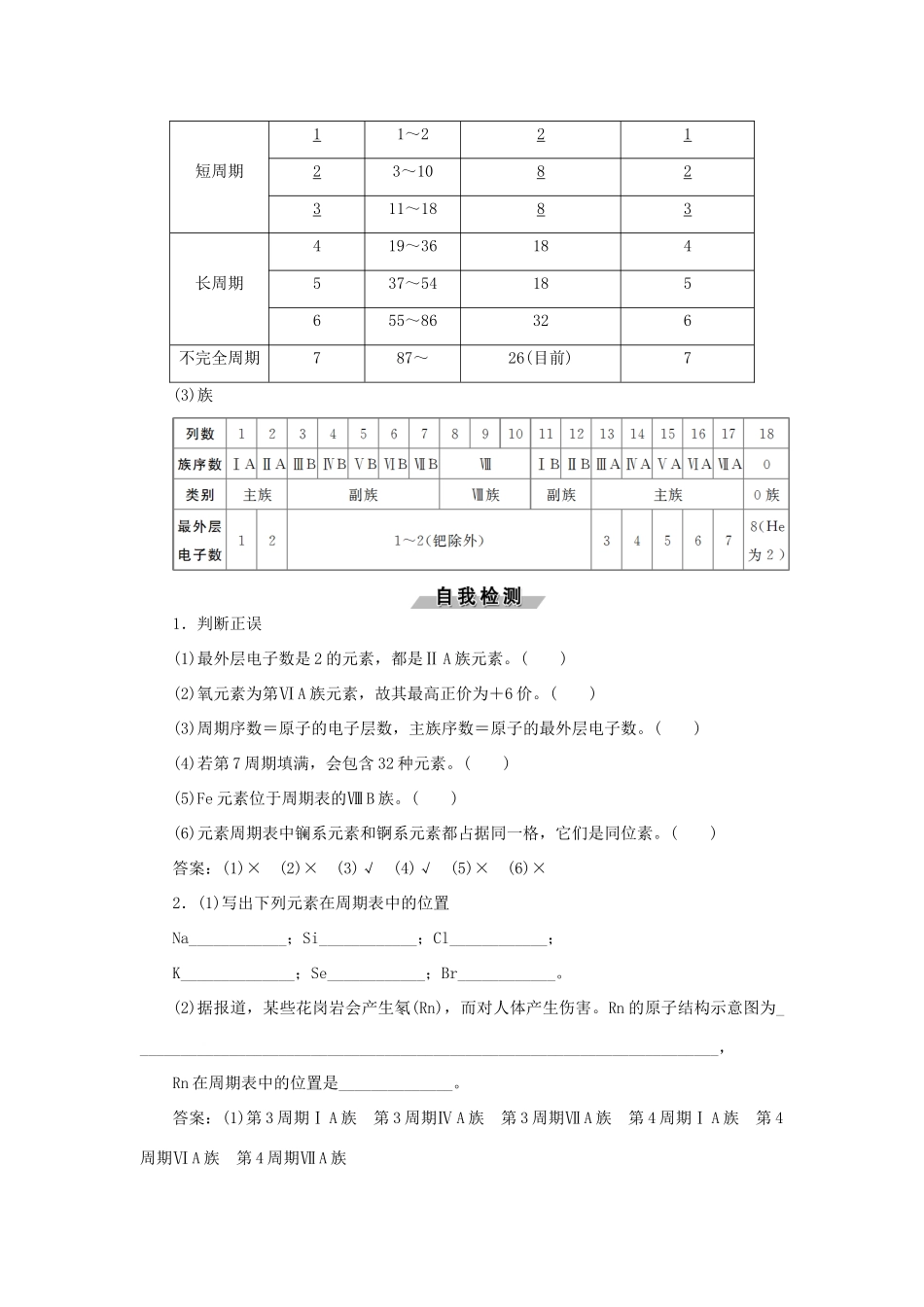
2.元素周期表的结构(1)元素周期表的编排原则①横行②纵列(2)周期周期类别周期序数起止元素原子序数包括元素种数核外电子层数短周期11~22123~1082311~1883长周期419~36184537~54185655~86326不完全周期787~26(目前)7(3)族1.判断正误(1)最外层电子数是2的元素,都是ⅡA族元素
()(2)氧元素为第ⅥA族元素,故其最高正价为+6价
()(3)周期序数=原子的电子层数,主族序数=原子的最外层电子数
()(4)若第7周期填满,会包含32种元素
()(5)Fe元素位于周期表的ⅧB族
()(6)元素周期表中镧系元素和锕系元素都占据同一格,它们是同位素
()答案:(1)×(2)×(3)√(4)√(5)×(6)×2.(1)写出下列元素在周期表中的位置Na____________;Si____________;Cl____________;K______________;Se____________;Br____________
(2)据报道,某些花岗岩会产生氡(Rn),而对人体产生伤害
Rn的原子结构示意图为________________________________________________________________________,Rn在周期表中的位置是______________
答案:(1)第3周期ⅠA族第3周期ⅣA族第3周期ⅦA族第4周期ⅠA族第4周期ⅥA族第4周期ⅦA族第6