阿伏加德罗定律及应用一、阿伏加德罗定律1
定义在相同温度相同压强下,相同体积的任何气体都含有相同数目的分子
阿伏加德罗定律只适用于气态物质
阿伏加德罗定律的条件是“三个相同”,即只有在同温、同压、同体积的条件下,才有分子数相同这一结论,而且是分子数相同,不是原子数相同
二、理想气体状态方程与阿伏加德罗定律1
理想气体状态方程a
式中T表示绝对温度,单位为开(K),摄氏温度与绝对温度的换算关系为;p表示大气压,单位为帕(Pa);V表示气体的体积,单位为升(L);n表示理想气体的物质的量;R为常数
(注:高中阶级不要求掌握理想气体状态方程,但用它可以更好地理解和应用阿伏加德罗定律
推导阿伏加德罗定律
由,可推知:、
当p、V、T均相同时,
三、应用例析【题目】常温下,在某容积固定的密闭容器里分别充入两种气体各,在一定条件下充分反应后,恢复至原温度,容器内气体的压强降为开始时的1/4,则原混合气体可能是A
和解析:V、T相同时,由、可推出:,,所以
即同温同体积条件下,气体的压强之比等于其物质的量之比
反应后气体的压强为反应前气体压强的1/4,说明反应后气体的总物质的量是反应前气体的总物质的量的1/4
常温下,与反应后生成的水为液态,剩余气体为未反应完的(),则反应后气体的总物质的量是反应前的,故A项正确
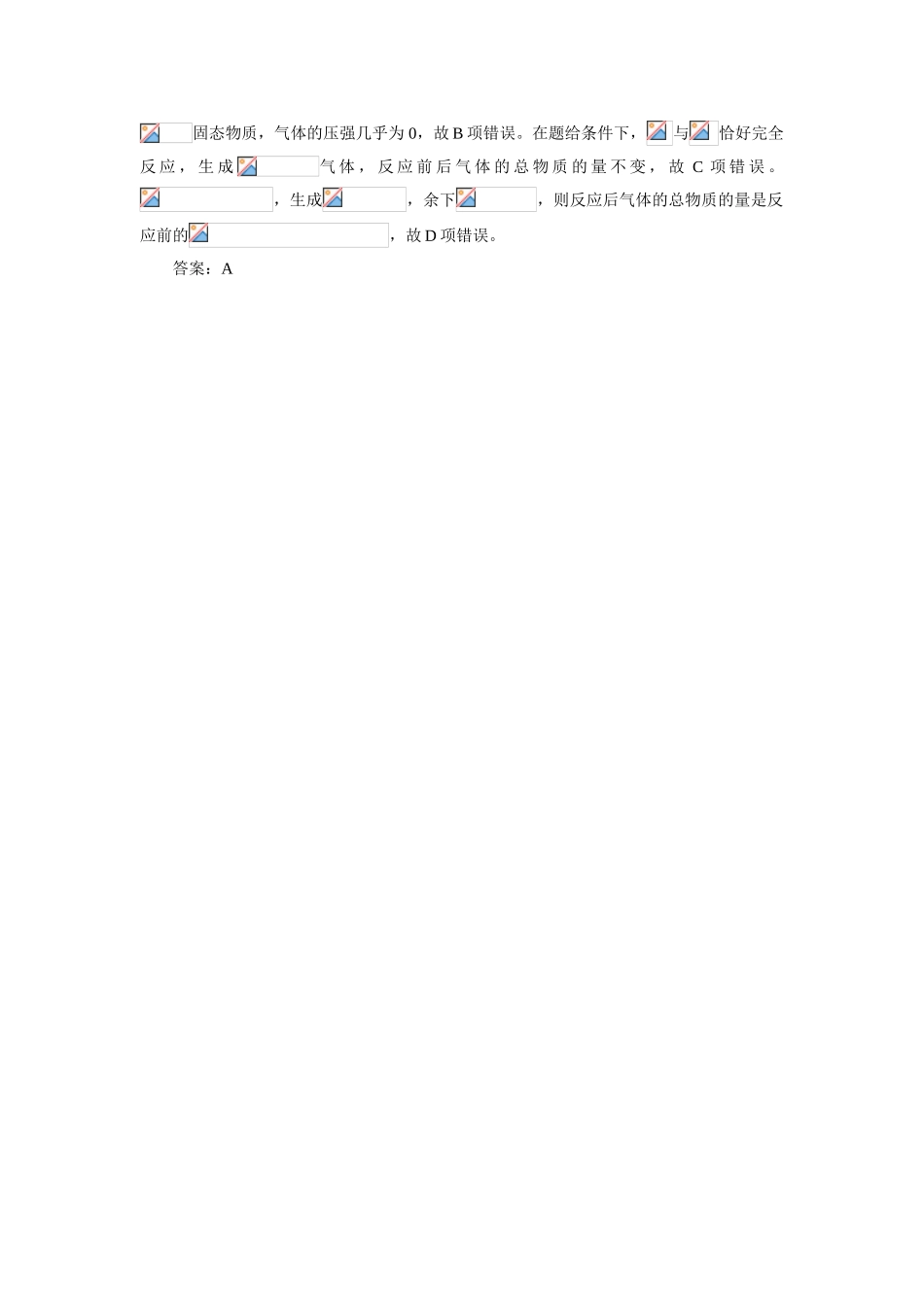
在题给条件下,与恰好完全反应,生成固态物质,气体的压强几乎为0,故B项错误
在题给条件下,与恰好完全反应,生成气体,反应前后气体的总物质的量不变,故C项错误
,生成,余下,则反应后气体的总物质的量是反应前的,故D项错误