浙江省温州市龙湾中学高三化学选择题专题训练14-化学反应与能量变化1、盖斯定律认为能量总是守恒的,化学反应过程一步完成或分步完成,整个过程的热效应是相同的
已知:①H2O(g)=H2O(1);△H1=-Q1kJ•mol-1②C2H5OH(g)=C2H2OH(1);△H2=-Q2kJ•mol-1③C2H2OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H3=-Q3kJ•mol-1,若使23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为(kJ)()A.Q1+Q2+Q3B.1
5Q3C.0.5Q1-1
5Q2+0.5Q3D.0.5(Q1+Q2+Q3)2、已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57
3kJ/mol下列结论正确的是()A.碳的燃烧热大于110
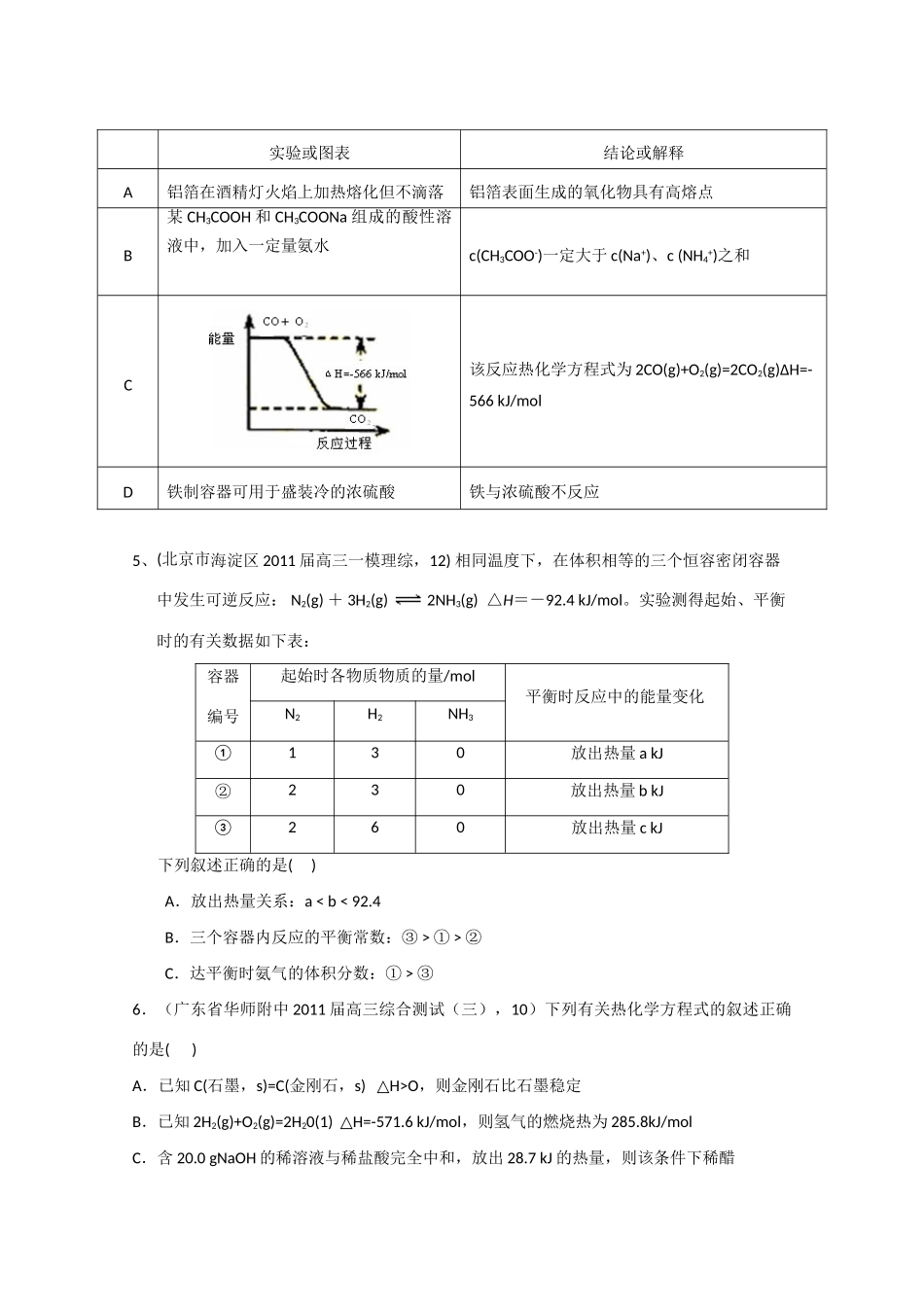
5kJ/molB.①的反应热为221kJ/molC.稀硫酸与稀NaOH溶液反应的中和热为-57
3kJ/molD.稀醋酸与稀NaOH溶液反应生成1mol水,放出57
3kJ热量3、甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:①2CH4(g)+O2(g)=2CO(g)+4H2(g);△H=-71kJ·mol-1②CO(g)+2H2(g)=CH3OH(l);△H=-90
5kJ·mol-1下列描述错误的是()A.CO(g)+2H2(g)==CH3OH(g)△H>-90
5kJ·mol-1B.在甲醇燃料电池中,甲醇所在电极为正极C.CH4(g)+1/2o2(g)===CH3(OH)(l)△H=-126kJ·mol-1D.反应①中的能量变化如右图所示4、下列实验或图表的结论或解释正确的是()5、(北京市海淀区2011届高三一模理综,12)相同温度下,在体积相等的三个恒容密闭