第四章晶体化学晶体化学--------研究晶体的化学成分与内部结构关系的一门学科
研究内容:(1)、组成晶体质点本身的特点(大小、电价、电子层结构);(2)、质点相互作用时所表现出来的现象和规律:▲质点的排列方式▲质点配位形式▲质点相互间的作用力-------化学键▲晶格类型紧密堆积:紧密堆积方式因充分利用了空间,而使体系的势能尽可能降低,从而结构更稳定
因为在离子键和金属键的晶体结构中,离子键和金属键是没有方向性的,核外电子云的分布是球形,可以作为球形来考虑
所以对于离子键和金属键的晶体结构,可以用球体最紧密堆积原理来研究
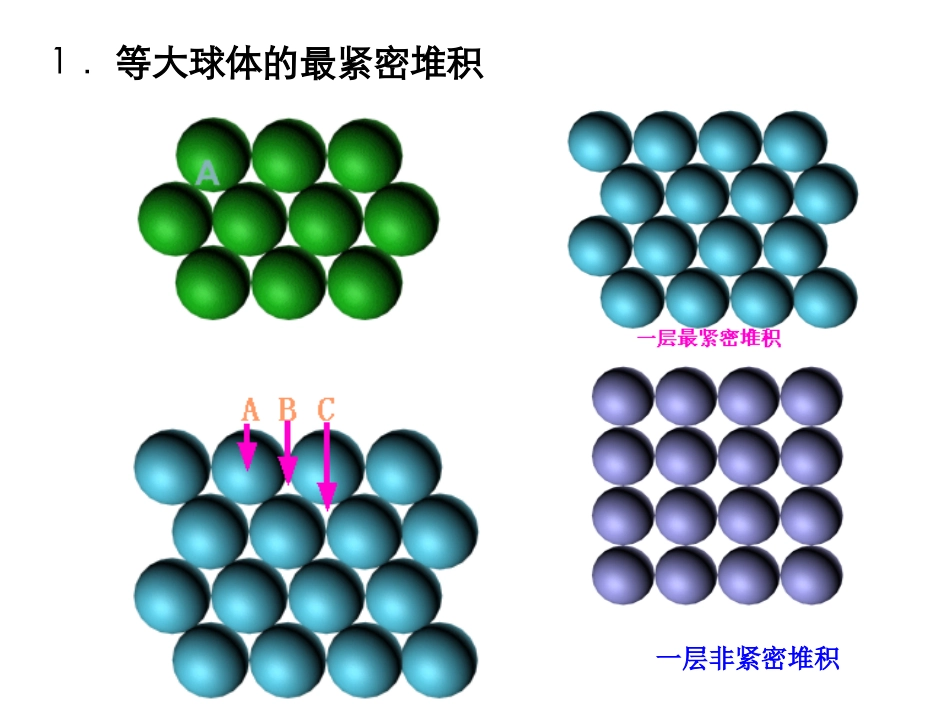
一、球体的紧密堆积原理1.等大球体的最紧密堆积一层非紧密堆积(1)六方最紧密堆积第三层堆积ABABABA(2)立方最紧密堆积CBAA2.不等大球体的最紧密堆积在晶体的离子化合物中,由于阴离子半径往往大于阳离子半径,所以在晶体结构中,常把阴离子当作最紧密堆积(空隙体积占25
95%)而把阳离子当作充填在空隙中
即:大球体作最紧密堆积,小球体充填在空隙中
例:NaCl晶体:Cl-作立方最紧密堆积,Na+充填在八面体空隙中
Cl-Na+n个等大球体作最密堆积,产生2n个四面体空隙n个八面体空隙,空隙体积占整个堆积体积的25
95%,四面体空隙八面体空隙二、配位数和配位多面体1
配位数----晶体结构中,一个原子或离子周围最邻近的,与之成配位关系的同种原子或异号离子的数目
N----coordinationnumber)例:NaCl晶体:C
NNa=62
配位多面体-----以一个原子或离子为中心,将其周围与之成配位关系的同种原子或异号离子的,中心联结起来,所获得的多面体,称为该原子或离子的配位多面体
配位多面体有多种形式,晶体结构常可看成是由配位多面体相互联结而成的一种体系
例:金刚石晶体结构(以配位多面体形式表示)金刚石配位多面体Cl-