新课标人教版选修四化学反应原理第四章电化学基础第一节原电池第一节原电池复习回顾1、原电池是______________________的装置
原电池反应的本质是_______________反应
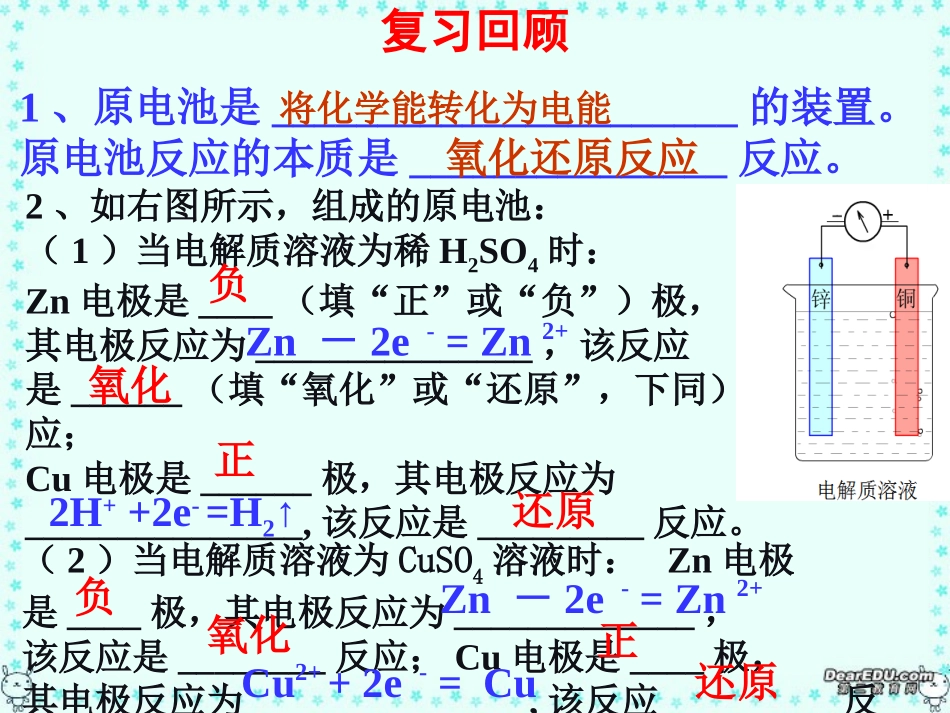
将化学能转化为电能氧化还原反应2、如右图所示,组成的原电池:(1)当电解质溶液为稀H2SO4时:Zn电极是____(填“正”或“负”)极,其电极反应为_______________,该反应是______(填“氧化”或“还原”,下同)反应;Cu电极是______极,其电极反应为_______________,该反应是_________反应
(2)当电解质溶液为CuSO4溶液时:Zn电极是____极,其电极反应为_____________,该反应是________反应;Cu电极是____极,其电极反应为_______________,该反应_________反应
负Zn-2e-=Zn2+氧化正2H++2e-=H2↑还原负Zn-2e-=Zn2+氧化正Cu2++2e-=Cu还原氧化反应Zn-2e=Zn2+铜锌原电池电解质溶液盐桥失e,沿导线传递,有电流产生还原反应2H++2e-=H2↑阴离子阳离子总反应:负极正极2H++2e-=H2↑Zn-2e-=Zn2+Zn+2H+=Zn2++H2↑Zn+H2SO4=ZnSO4+H2↑(离子方程式)(化学方程式)电极反应正极:负极:(氧化反应)(还原反应)阳离子原电池原理原电池原理外电路内电路与与原电池相关的概原电池相关的概念念1
电路:外电路内电路电子流向:负极流向正极电流方向:正极流向负极阴离子流向负极阳离子流向正极2
电极:正极:电子流入的一极负极:电子流出的一极3
电极反应式:正极:2H++2e-=H2↑负极:Zn-2e-=Zn2+4
总反应式:Zn+2H+=Zn2++H2↑
提出问题:上图是我们在必修2中学习过的将锌片和铜片置于稀硫酸的原电池,