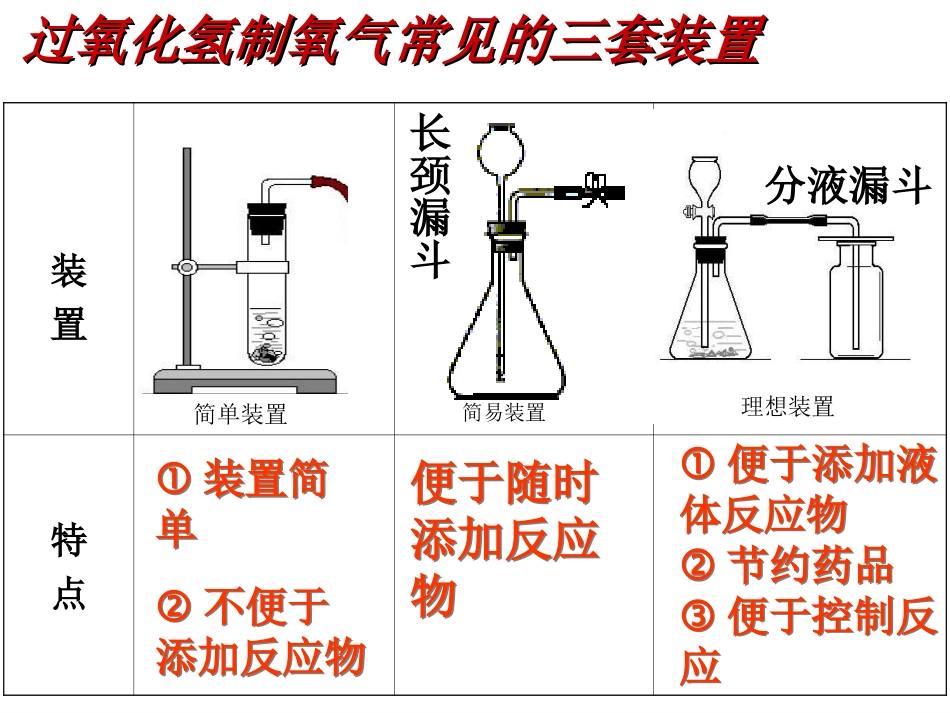
课题3制取氧气二、分解过氧化氢制取氧气:1、实验原理:过氧化氢水+氧气二氧化锰2、实验装置:过氧化氢制氧气常见的三套装置过氧化氢制氧气常见的三套装置装置特点装置简单不便于添加反应物装置简单不便于添加反应物便于随时添加反应物便于随时添加反应物便于添加液体反应物节约药品便于控制反应便于添加液体反应物节约药品便于控制反应简单装置分液漏斗理想装置长颈漏斗简易装置注意事项:1、固体药品应事先直接加入锥形瓶中;2、长颈漏斗的作用是加入液体药品;3、长颈漏斗的下端管口应伸入液面以下(液封作用)4、锥形瓶中的导气管不应伸入反应液面以下,应刚露出胶塞为宜;——长颈漏斗3、实验步骤:⑴按要求组装好仪器;⑵检查装置气的密性;⑶向锥形瓶加入二氧化锰,向长颈漏斗内加入过氧化氢溶液;⑷收集气体
步骤一:在常温下,把带火星的木条伸入过氧化氢溶液的试管,观察木条是否复燃
现象:带火星的木条不能复燃,结论:常温下过氧化氢溶液分解很慢,放出氧气少
探究:过氧化氢(H2O2)溶液制取氧气步骤二:向上述试管中,加入少量二氧化锰,把带火星的木条伸入试管
观察发生的现象
现象:带火星的木条复燃了结论:常温下二氧化锰(MnO2)加速了过氧化氢溶液的分解,放出的氧气使带火星的木条复燃
步骤三:反应停止后,重新加入过氧化氢溶液,把带火星的木条伸入试管
观察发生的现象
现象:带火星的木条复燃了结论:二氧化锰(MnO2)仍然在起作用使过氧化氢溶液分解产生氧气
4、催化剂:在化学反应里能改变其他物质的化学反应速率,而本身质量和化学性质在化学反应前后都没有发生变化的物质
催化剂的特点一变:化学反应速率变二不变:质量不变、化学性质不变5、催化剂应掌握⑴改变速率包括加快和减慢;⑵化学性质和质量匀未改变,物理性质会改变;⑶对某具体反应可作催化剂,并不是任何时候都作催化剂
⑷同一反应可能有多种催化剂
⑸不能改变生成物的