受试者编号:□□□□XXXXXXXXXXX(此处输入课题名称)XXXXXXXXXXX病例报告表(CaseReportForm)受试者姓名缩写:□□□□研究医师:所在科室:研究单位:研究开始日期:年月日研究结束日期:年月日填表说明在正式填表前,请认真阅读下列填表说明1
筛选合格者填写正式病例报告表
病例报告表应用签字笔填写
3病例填写务必准确、清晰,不得随意涂改,错误之处纠正时需用横线居中划出,并签署修改者姓名缩写及修改时间
8LGW05-02-12
患者姓名拼音缩写四格需填满,两字姓名填写两字拼音前两个字母;三字姓名填写三字首字母及第三字第二字母;四字姓名填写每一个字的首字母
举例:张红Z|H|H|O;李淑明L|S|M|I;欧阳小惠O|Y|X|H5
所有选择项目的□内用√标注
表格中所有栏目均应填写相应的文字或数字,不得留空
因故未查或漏查,请填写“ND”;具体用药剂量和时间不明,请填写“NK”;不适用请选“NA”
期间应如实填写不良事件记录表
记录不良事件的发生时间、严重程度、持续时间、采取的措施和转归
如有严重不良事件发生(包括临床研究过程中发生需住院治疗、延长住院时间、伤残、影响工作能力、危及生命或死亡、导致先天畸形等事件),必须立即通知主要研究者及其单位伦理委员会
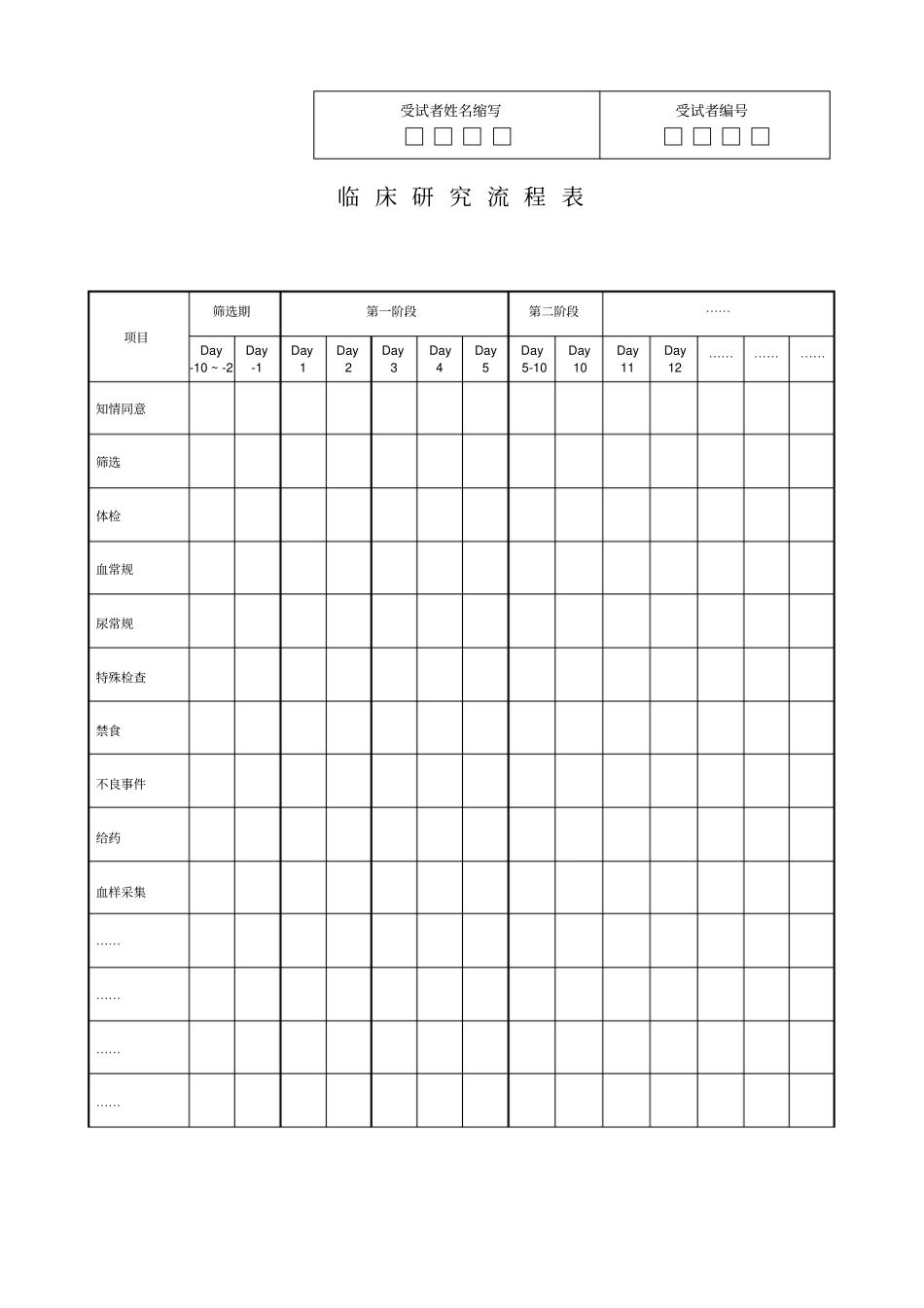
临床研究流程表受试者姓名缩写□□□□受试者编号□□□□项目筛选期第一阶段第二阶段⋯⋯Day-10~-2Day-1Day1Day2Day3Day4Day5Day5-10Day10Day11Day12⋯⋯⋯⋯⋯⋯知情同意筛选体检血常规尿常规特殊检查禁食不良事件给药血样采集⋯⋯⋯⋯⋯⋯⋯⋯筛选期记录受试者是否符合入选标准1、按研究方案填写是□否□2、⋯⋯是□否□3、是□否□4、是□否□5、是□否□6、是□否□如果以上任何一项回答是“否”,则受试者不能进入研究