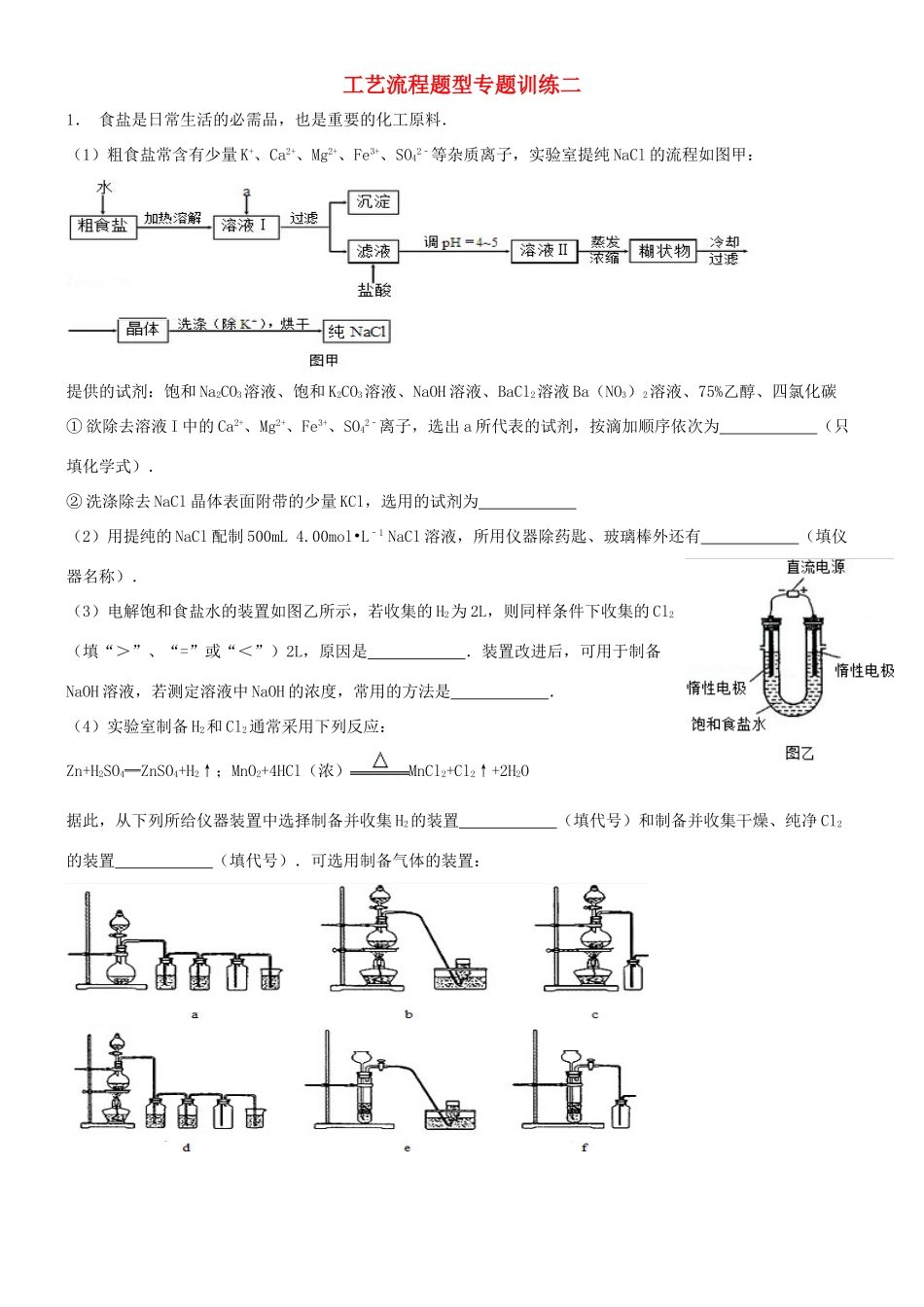
工艺流程题型专题训练二1.食盐是日常生活的必需品,也是重要的化工原料.(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42﹣等杂质离子,实验室提纯NaCl的流程如图甲:提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液Ba(NO3)2溶液、75%乙醇、四氯化碳①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42﹣离子,选出a所代表的试剂,按滴加顺序依次为(只填化学式).②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为(2)用提纯的NaCl配制500mL4
00mol•L﹣1NaCl溶液,所用仪器除药匙、玻璃棒外还有(填仪器名称).(3)电解饱和食盐水的装置如图乙所示,若收集的H2为2L,则同样条件下收集的Cl2(填“>”、“=”或“<”)2L,原因是.装置改进后,可用于制备NaOH溶液,若测定溶液中NaOH的浓度,常用的方法是.(4)实验室制备H2和Cl2通常采用下列反应:Zn+H2SO4═ZnSO4+H2↑;MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O据此,从下列所给仪器装置中选择制备并收集H2的装置(填代号)和制备并收集干燥、纯净Cl2的装置(填代号).可选用制备气体的装置:2.聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3﹣0
5n]m,广泛用于污水处理.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4•7H2O),过程如图1:(1)验证固体W焙烧后产生的气体含有SO2的方法是:.(2)实验室制备、收集干燥的SO2,所需仪器如图2.装置A产生SO2,按气流方向连接各仪器接口,顺序为a→→→→→f.装置A中发生反应的化学方程式为.(3)制备绿矾时,向溶液X中加入过量,充分反应后,经过滤操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾.过滤所需的玻璃仪