碳族元素知识归纳二
教学目标:1
通过对比归纳C和Si;和等主要单质和化合物的性质
归纳酸式盐的有关反应
连续反应的讨论题
知识体系:1
碳族元素(1)概述①结构:最外层都是4个电子②位置:ⅣA族(2)性质①相似性:化合价,易形成共价化合物,难形成简单离子②递变性:从,非金属性逐渐减弱,金属性逐渐增强2
Si(1)物理性质:熔沸点高,硬度大,半导体(2)化学性质:①常温:只与、强碱溶液反应②加热:与等反应(3)制备:3
(1)物理性质:硬度大,熔沸点高(2)化学性质:①酸性氧化物,具有酸性氧化物的通性②不与水反应(不溶于水)③不与酸反应(HF除外)④高温下与等反应生成相应的硅酸盐⑤与强碱反应:4
硅酸盐工业及新型无机非金属材料四
专题总结:专题一常见试剂的保存(见下表)类别常见药品有关特性保存方法空气中易变质(1)Na、K易跟、水反应煤油中(2)、漂白粉易跟、水反应密封(3)溶液、石灰水、水玻璃易跟反应,粘合玻璃密封,要用橡胶塞,不用玻璃塞(4)易风化失去结晶水密封(5)浓硫酸易吸水、强氧化性密封,不用橡胶塞见光易变质氯水、、见光易分解、有强氧化性棕色瓶中,冷暗处,不用橡胶塞易燃(1)镁、硫遇火易燃远离火种,单独存放(2)汽油、酒精、苯易燃有机溶剂远离火种,不用橡胶塞易爆、受热易分解、强氧化性远离易燃物,防受热冲击强腐蚀性(1)液溴易挥发的强氧化剂棕色瓶中,玻璃塞,水封(2)氢氟酸腐蚀玻璃塑料瓶中专题二碳与硅单质的性质比较1
金刚石和晶体硅都是原子晶体,都不溶于水和任何有机溶剂,它们的熔、沸点、硬度均高,但前者比后者更高
碳、硅在常温下稳定,高温时活泼性增强,主要表现还原性
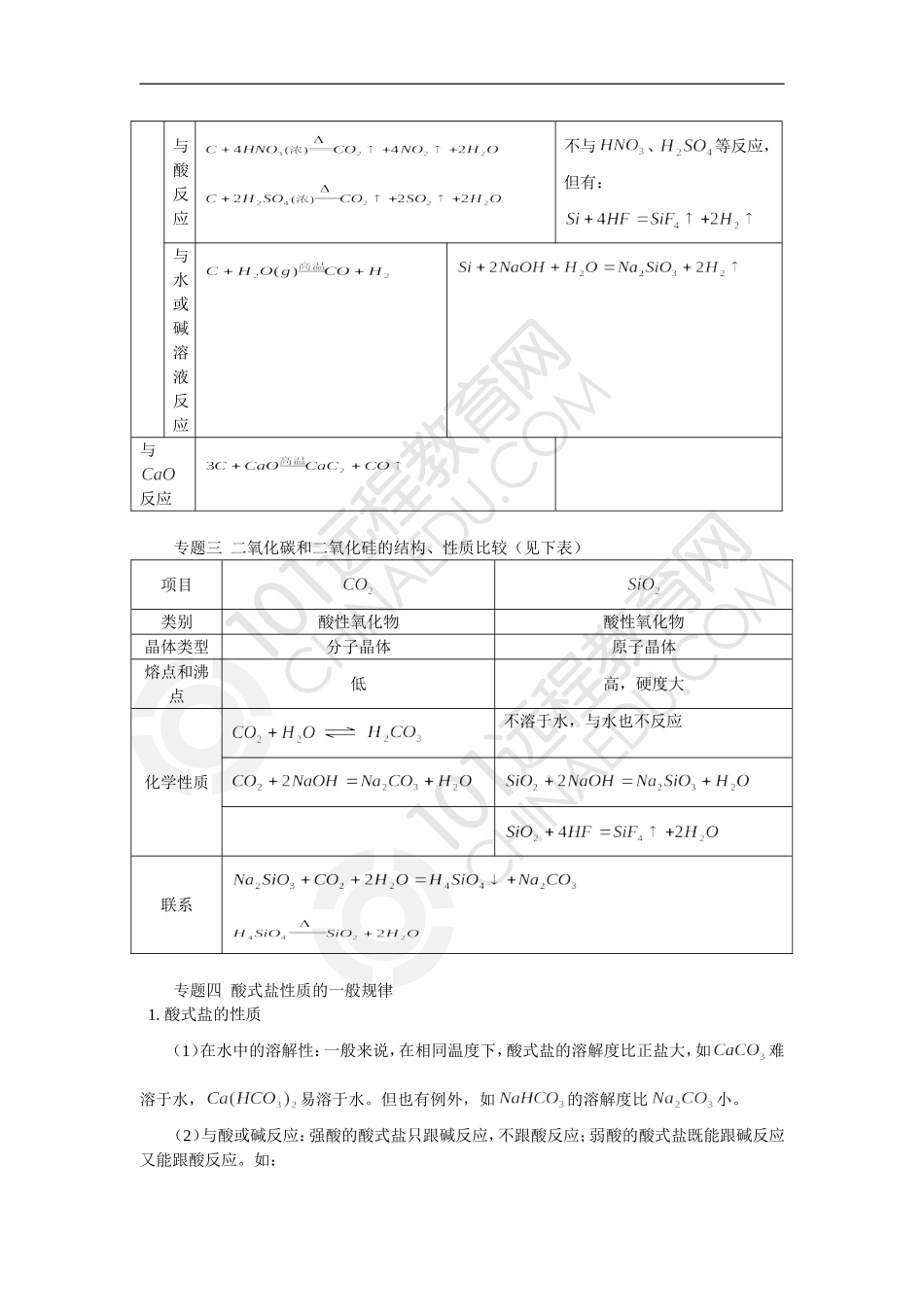
碳、硅的化学性质(见下表)
碳和硅的性质比较化学性质碳硅还原性与单质反应(不稳定)与氧化物反应与酸反应不与、等反应,但有:与水或碱溶液反应与反应专题三二氧化碳和二氧化硅的结构、性质比较(