初三化学数据分析题的解题妙招唐玉芳随着新课程的推进,化学数据分析题逐渐成为各地中考的命题热点
在这里介绍一种如何从考生的角度,掌握分析这类题的好方法
例1、在一个密闭容器内有X、Y、Z、Q4种物质,在一定条件下充分反应
测得反应前后各物质的质量如下:物质XYZQ反应前的质量/g01602050反应后的质量/g222026则该密闭容器中发生的化学反应类型为()
A、化合B、分解C、置换D、复分解解析:为了使同学们能具体地感知数据的变化及理解数据变化的化学意义,在图表行中加一行数据差栏
物质XYZQ反应前的质量/g01602050反应后的质量/g222026反应前后的质量差/g+222-160-18-44(反应前后的质量差/g)为正值则为生成物,(反应前后的质量差/g)为负值则为反应物
反应前后的质量差值符合质量守恒定律:160+18+44=222,即化学反应方程式为:Y+Z+Q=X
由以上分析推断,该密闭容器中发生的化学反应类型为化合反应
答案:A例2、有一种只含杂质(不溶于水,也不与盐酸反应)的石灰石样品
某学生想测定该样品中碳酸钙的质量分数,他取用2g样品,把16g稀盐酸平均分4次加入,充分反应后剩余固体的质量依次记录于下表:稀盐酸的用量/g剩余固体的质量/g第一次加入41
4第二次加入40
8第三次加入40
5第四次加入40
5计算:(1)样品中碳酸钙的质量分数;(2)2g样品与稀盐酸充分反应时,恰好用去稀盐酸的质量为多少克
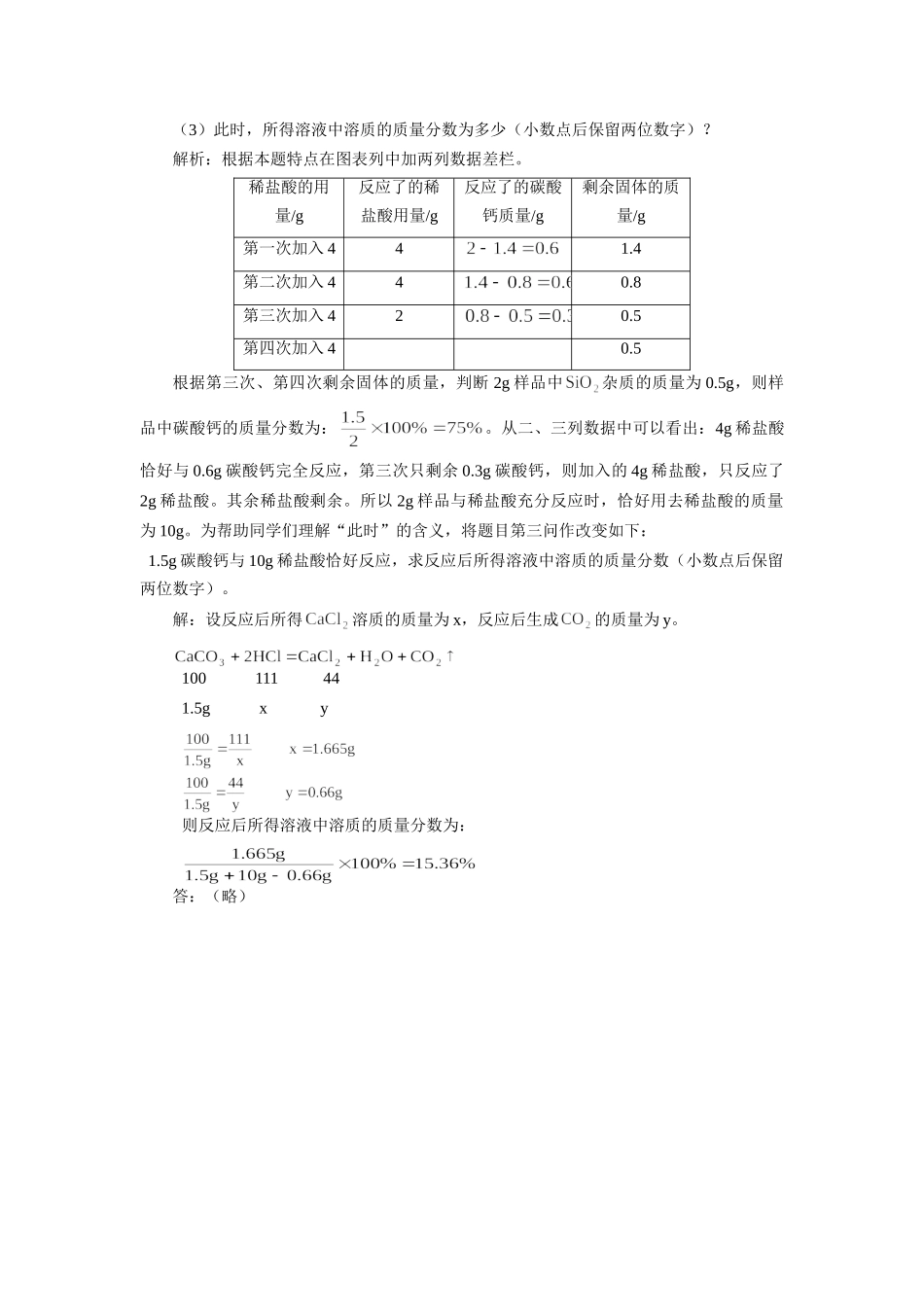
(3)此时,所得溶液中溶质的质量分数为多少(小数点后保留两位数字)
解析:根据本题特点在图表列中加两列数据差栏
稀盐酸的用量/g反应了的稀盐酸用量/g反应了的碳酸钙质量/g剩余固体的质量/g第一次加入441
4第二次加入440
8第三次加入420
5第四次加入40
5根据第三次、第四次剩余固体的质量,判断2g样品中杂质的质量为0
5g,则样品中碳酸