第四节研究有机化合物的一般步骤和方法第1课时有机化合物的分离、提纯课时演练·促提升A组1
下列各组混合物中,可以用分液漏斗分离的是()A
乙醇和乙酸C
溴苯和苯解析:溴苯和水为互不相溶的液体,可以用分液法分离,A项正确;B、C、D项均为互溶的液体混合物
将CH3CHO(易溶于水,沸点为20
8℃的易挥发性液体)和CH3COOH分离的最佳方法是()A
加入Na2CO3后,通过萃取的方法分离C
加入烧碱溶液之后蒸出乙醛,再加入硫酸,蒸出乙酸D
和Na反应后进行分离解析:乙醛沸点为20
8℃,而乙酸沸点为117
9℃,因此C选项的方法分离效果更好
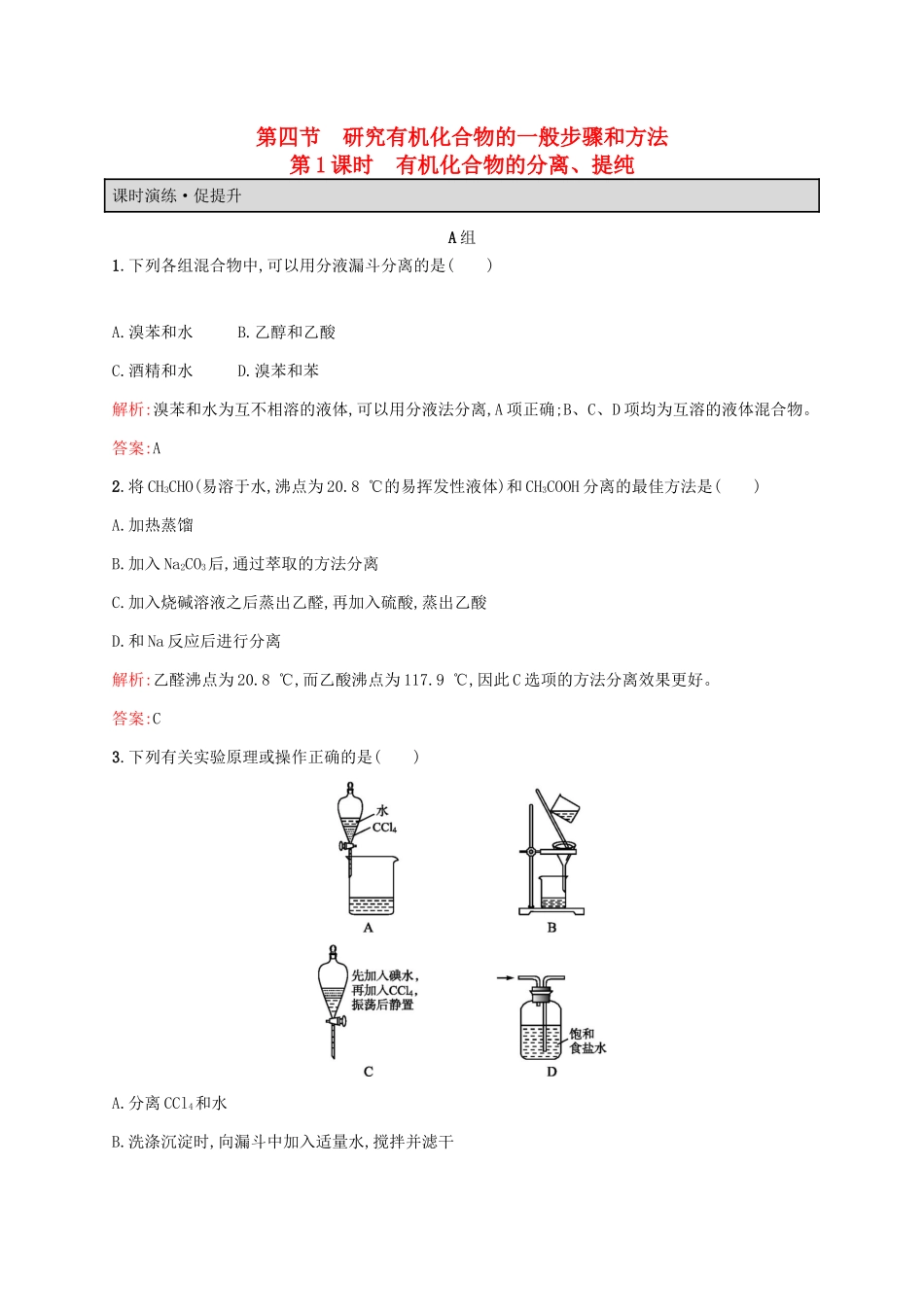
下列有关实验原理或操作正确的是()A
分离CCl4和水B
洗涤沉淀时,向漏斗中加入适量水,搅拌并滤干C
液体分层,下层呈无色D
除去氯气中的氯化氢解析:水与四氯化碳不互溶,可以用分液的方法除去,A项正确;在洗涤沉淀时加入的水要没过沉淀,但不能超过滤纸上沿,且不能搅拌,B项错误;四氯化碳的密度比水的密度大,在水的下面,C项错误;洗气应是长进短出,应从右侧通入,D项错误
下列物质中各含有少量的杂质,能用饱和碳酸钠溶液并借助于分液漏斗除去杂质的是()A
苯中含有少量甲苯B
乙醇中含有少量乙酸C
溴苯中含有少量苯D
乙酸乙酯中含有少量的乙酸解析:乙酸乙酯不溶于水且在饱和Na2CO3溶液中溶解度降低,而乙酸可溶于Na2CO3溶液,并与之反应,从而分层,可用分液法分离
化学工作者从有机反应RH+Cl2(g)RCl(l)+HCl(g)中受到启发,提出的在农药和有机合成工业中可获得副产品的设想已成为事实,试指出从上述反应产物中分离得到盐酸的最佳方法是()A
水洗分液法B
有机溶剂萃取法解析:利用HCl极易溶于水,而有机物一般难溶于水的特征,采用水洗分