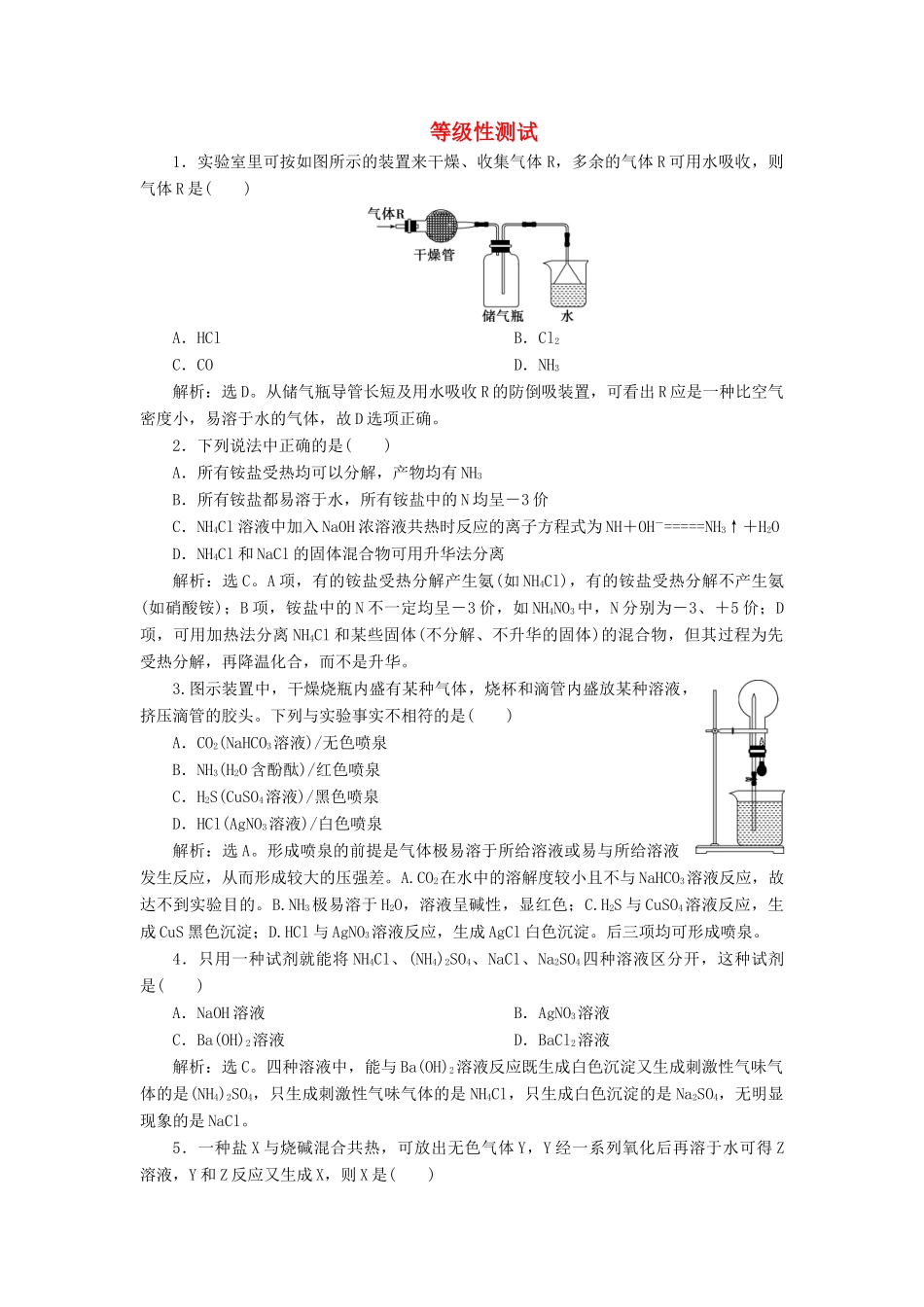
等级性测试1.实验室里可按如图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则气体R是()A.HClB.Cl2C.COD.NH3解析:选D
从储气瓶导管长短及用水吸收R的防倒吸装置,可看出R应是一种比空气密度小,易溶于水的气体,故D选项正确
2.下列说法中正确的是()A.所有铵盐受热均可以分解,产物均有NH3B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价C.NH4Cl溶液中加入NaOH浓溶液共热时反应的离子方程式为NH+OH-=====NH3↑+H2OD.NH4Cl和NaCl的固体混合物可用升华法分离解析:选C
A项,有的铵盐受热分解产生氨(如NH4Cl),有的铵盐受热分解不产生氨(如硝酸铵);B项,铵盐中的N不一定均呈-3价,如NH4NO3中,N分别为-3、+5价;D项,可用加热法分离NH4Cl和某些固体(不分解、不升华的固体)的混合物,但其过程为先受热分解,再降温化合,而不是升华
图示装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液,挤压滴管的胶头
下列与实验事实不相符的是()A.CO2(NaHCO3溶液)/无色喷泉B.NH3(H2O含酚酞)/红色喷泉C.H2S(CuSO4溶液)/黑色喷泉D.HCl(AgNO3溶液)/白色喷泉解析:选A
形成喷泉的前提是气体极易溶于所给溶液或易与所给溶液发生反应,从而形成较大的压强差
CO2在水中的溶解度较小且不与NaHCO3溶液反应,故达不到实验目的
NH3极易溶于H2O,溶液呈碱性,显红色;C
H2S与CuSO4溶液反应,生成CuS黑色沉淀;D
HCl与AgNO3溶液反应,生成AgCl白色沉淀
后三项均可形成喷泉
4.只用一种试剂就能将NH4Cl、(NH4)2SO4、NaCl、Na2SO4四种溶液区分开,这种试剂是()A.NaOH溶液B.AgNO3溶液C.Ba(OH)2溶液D.BaCl2溶液解析:选C