1 / 10 第十一章化学动力学一、主要概念反应速率,依时计量学反应,(非依时计量学反应, )消耗速率,生成速率,基元反应,非基元反应,质量作用定律,级数,总级数,(基元反应的 )反应分子数,速率方程,半衰期,反应级数的确定方法(积分法,微分法,初浓度法,隔离法,半衰期法 ),活化能,指前因子,速率常数,表观活化能或经验活化能2,对行反应,平行反应,连串反应,稳态处理法,平衡态近似法,单分子反应机理,直链反应,支链反应,爆炸,碰撞理论要点,势能面,反应途径,过渡状态理论要点
笼罩效应,遭遇对,量子效率,催化剂二、主要定义式与公式1.反应速率:标准反应0=B vB B ,反应进度: dξ=dnB /vB , 反应速率: r = dξ /Vdt =dnB/ V vBdt =(恒V)dcB/vBdtr 生成速率 (反应物 ):r B = - dcB/ dt 消耗速率 (产物):r B = dcB/ dt 2.质量作用定律:对基元反应aA + bB +
→ lL +mM 速率方程: - dcA/dt = k cAa cBb
速率方程的一般形式:经验式:- dcA/dt = k cAcB
(微分式 ) 式中:、反应物 A,B的分级数,反应的总级数 n=;k- 速率常数,与温度有关
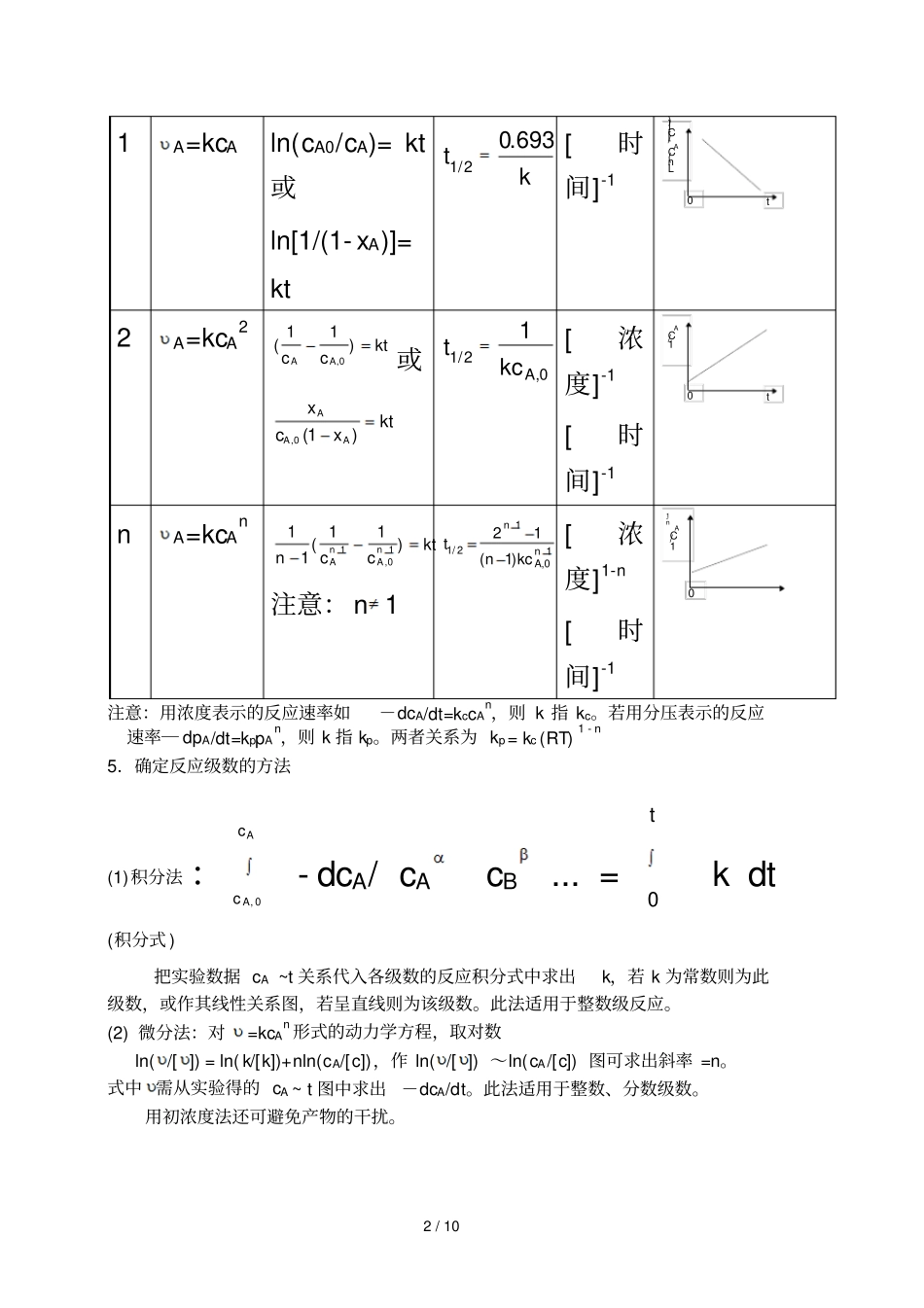
4.简单级数反应的动力学特征表、简单反应浓度对反应速率的影响级数微分式积分式半衰期k 量纲线形关系式0 A=kcA0- cA= kttckA1 202/,[浓度] [时间]-1t0CA,0-CA2 / 10 1 A=kcAln(cA0/cA)= kt或ln[1/(1- xA)]=kttk1 20 693/
[时间]-1t0Ln(CA/[C])2 A=kcA2(),110ccktAA或xcxktAAA, ()0 1tkcA1 201/,[浓度]-1 [时间]-1t01/CAnA=kc