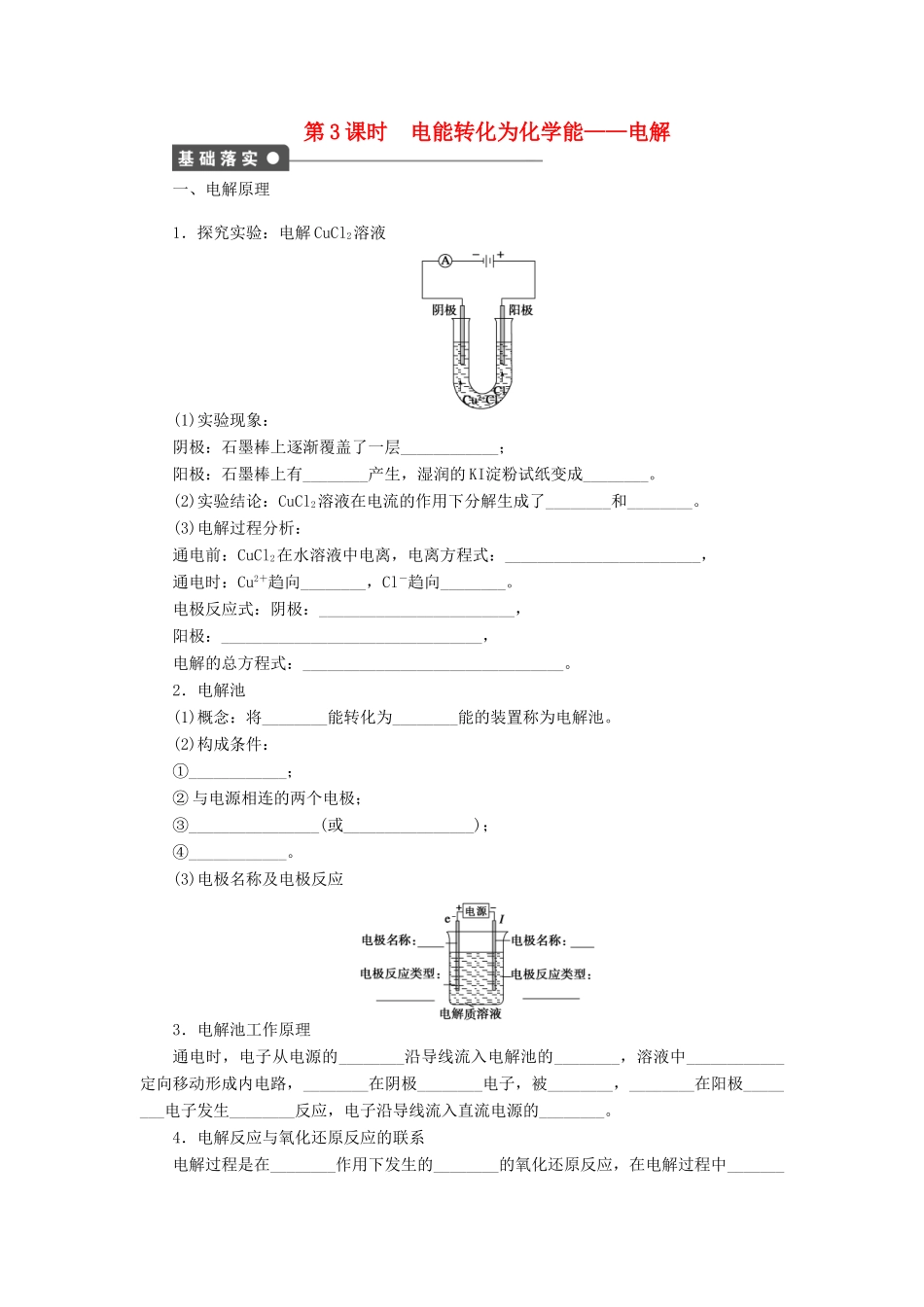
第 3 课时 电能转化为化学能——电解一、电解原理1.探究实验:电解 CuCl2溶液(1)实验现象:阴极:石墨棒上逐渐覆盖了一层____________;阳极:石墨棒上有________产生,湿润的 KI淀粉试纸变成________
(2)实验结论:CuCl2溶液在电流的作用下分解生成了________和________
(3)电解过程分析:通电前:CuCl2在水溶液中电离,电离方程式:________________________,通电时:Cu2+趋向________,Cl-趋向________
电极反应式:阴极:________________________,阳极:________________________________,电解的总方程式:________________________________
2.电解池(1)概念:将________能转化为________能的装置称为电解池
(2)构成条件:①____________;② 与电源相连的两个电极;③________________(或________________);④____________
(3)电极名称及电极反应3.电解池工作原理通电时,电子从电源的________沿导线流入电解池的________,溶液中____________定向移动形成内电路,________在阴极________电子,被________,________在阳极________电子发生________反应,电子沿导线流入直流电源的________
4.电解反应与氧化还原反应的联系电解过程是在________作用下发生的________的氧化还原反应,在电解过程中________转化为________,从而使许多情况下不能发生的反应得以进行,这对于化工生产、金属冶炼、科学研究以及人们日常生活都具有十分重要的意义