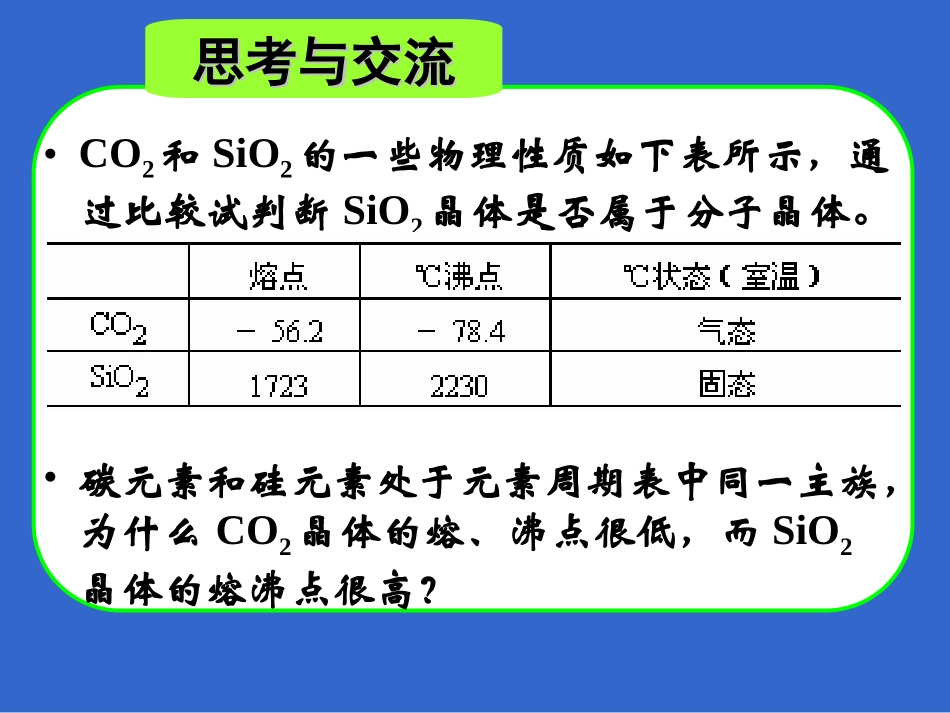
第二节分子晶体和原子晶体第二课时思考与交流思考与交流•CO2和SiO2的一些物理性质如下表所示,通过比较试判断SiO2晶体是否属于分子晶体
•碳元素和硅元素处于元素周期表中同一主族,为什么CO2晶体的熔、沸点很低,而SiO2晶体的熔沸点很高
二氧化硅的晶体结构SiO共价键一、原子晶体(共价晶体)1、定义:相邻原子间均以共价键相结合而形成空间立体网状结构的晶体
构成微粒:微粒间的相互作用:熔化时需克服的作用:原子共价键共价键注意注意原子晶体中不存在单个分子,没有分子式
原子晶体中不存在单个分子,没有分子式
SiOSiO22是表示晶体中是表示晶体中SiSi、、OO原子数之比是原子数之比是1:21:2的化学式的化学式对比分子晶体和原子晶体的数据,原子晶体有何物理特性
在原子晶体中,由于原子间以较强的共价键相结合,而且形成空间立体网状结构,所以原子晶体的2
原子晶体的物理特性原子晶体的物理特性(1)熔点和沸点高(2)硬度大(3)一般不导电(4)且难溶于一些常见的溶剂思考:金刚石的结构特征:1、金刚石晶体中每个碳原子与它直接相邻的___个碳原子形成____结构,其碳原子的杂化类型为___,C-C-C的夹角为___2、金刚石晶体中平均每个碳原子形成__个C-C键,所以金刚石中碳原子数与C-C键数之比为___,12g金刚石中C—C键数为___NA个4正四面体sp3109º28´21:22•3
常见的原子晶体•某些非金属单质:•金刚石(C)、晶体硅(Si)、晶体硼(B)、晶体锗(Ge)等•某些非金属化合物:•碳化硅(SiC)晶体、氮化硼(BN)晶体•某些氧化物:•二氧化硅(SiO2)晶体、Al2O3若以硅原子代替金刚石晶体结构中的碳原子,便可得到晶体硅的结构,不同的是硅晶体中的Si-Si键的键长比金刚石中的C-C键长作为晶体管材料109º28´SiO共价键若在硅晶体结构中的每个Si-S