配合物与沉淀-溶解平衡一、实验目的1
加深理解配合物的组成和稳定性,了解配合物形成时的特征;2
加深理解沉淀-溶解平衡和溶度积的概念,掌握溶度积规则及其应用;3
初步学习分离常见混合阳离子
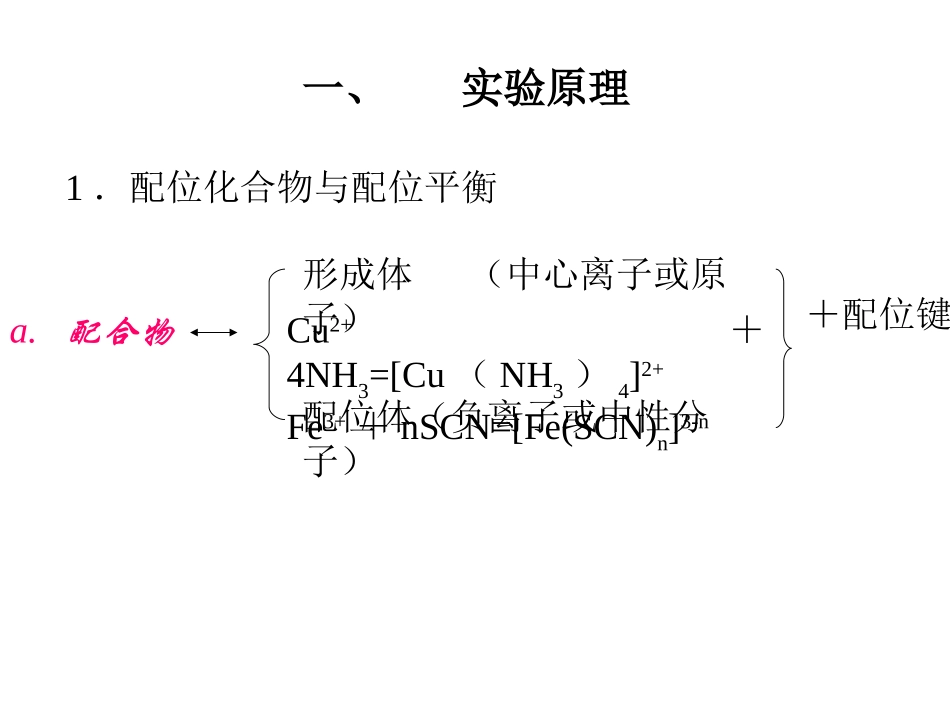
一、实验原理1.配位化合物与配位平衡a
配合物形成体(中心离子或原子)Cu2++4NH3=[Cu(NH3)4]2+Fe3++nSCN=[Fe(SCN)n]3-n配位体(负离子或中性分子)+配位键b
配合物生成配合物生成取代:[Fe(SCN)n]3-n+6F-[FeF6]3-+nSCN-加成:HgI2(s)+2I-[HgI4]2-2
沉淀-溶解平衡溶度积常数:Kspθ(AmBn)=[c(An+)/cθ]m[c(Bm-)/cθ]nAmBn(s)mAn++nBm-Kspθ(AmBn)=[c(An+)/cθ]m[c(Bm-)/cθ]na
Jθ>Kspθb
Jθ=Kspθc
Jθ<Kspθ一、仪器、药品仪器:试管、试管架、离心试管、离心机药品参见课本四、实验步骤以下有的方程未配平切勿照抄
以下只是理论分析不要根据此讲义修改原始记录
1.(1)32[]()FeSCNFeSCN血红色的标准稳定常数教材p656页2[]FeSCN29
110fK36FeF的标准稳定常数67
110fK所以加入氟离子后会发生如下转化远远大于前者3366FeFFeF(无色)(2)3K�+3-366K[Fe(CN)]电离+[Fe(CN)](深红色)稳定常数524
110fK极稳定
滴入KSCN,不会发生变化
442()NHFeSO是一种复盐,教材p140页
32[]()FeSCNFeSCN血红色会电离出三价铁离子,滴入KSCN(3)222443[(3)]CuNHHOCuNH(蓝色)(深蓝色)加入NaOH无变化说明二价铜离子发生了络合加入BaCl2,生成硫酸钡