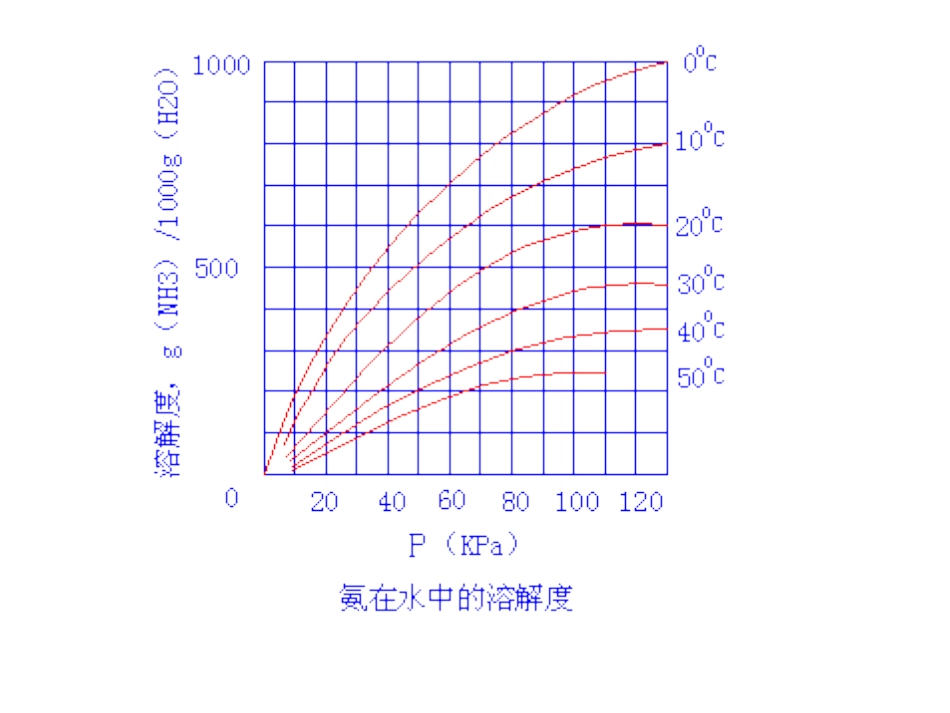
第六章吸收一、气体的溶解度二、亨利定律三、用气液平衡关系分析吸收过程第二节第二节气液相平衡气液相平衡一、气体的溶解度1、气体在液体中溶解度的概念气体在液相中的溶解度:2、溶解度曲线气体在液体中的饱和浓度*AC•吸收剂、温度T、P一定时,不同物质的溶解度不同
•温度、溶液的浓度一定时,溶液上方分压越大的物质越难溶
•对于同一种气体,分压一定时,温度T越高,溶解度越小
•对于同一种气体,温度T一定时,分压P越大,溶解度越大
•加压和降温对吸收操作有利
二、亨利定律1、亨利定律Exp*E——亨利系数,单位与压强单位一致
E值取决于物系的特性及温度;温度T上升,E值增大;在同一溶剂中,E值越大的气体越难溶
2、亨利定律的其他表示形式1)用溶质A在溶液中的摩尔浓度和气相中的分压表示的亨利定律Hcp*H——溶解度系数,单位:kmol/m3·Pa或kmol/m3·atm
H是温度的函数,H值随温度升高而减小
易溶气体H值大,难溶气体H值小
H与E的关系设溶液的密度为3/mkg,浓度为3/mkmolC总,则MC总SSAAxMxMM对于稀溶液,SSMM,ECH总EMss2)气液相中溶质的摩尔分数表示的亨利定律mxy*m——相平衡常数,是温度和压强的函数
温度升高、总压下降则m值变大,m值越大,表明气体的溶解度越小
m与E的关系:yPp由分压定律知:Ppy*xEp*由亨利定律:xPEyPEm即:3)用摩尔比Y和X分别表示气液两相组成的亨利定律a)摩尔比定义:液相中溶剂的摩尔数液相中溶质的摩尔数Xxx1数气相中惰性组分的摩尔气相中溶质的摩尔数Yyy1YYyXXx1,1由,*得mxyxmxYY11**xmmxY)1(1*当溶液浓度很低时,X≈0,上式简化为:mXY*亨利定律的几种表达形式也可改写为HPcEPx