实验二十主族金属(碱金属、碱土金属、铝、锡、铅、锑、铋)实验目的•比较碱金属、碱土金属的活泼性;•试验并比较碱土金属、铝、锡、铅、锑、铋的氢氧化物和盐类的溶解性;•练习焰色反应并熟悉使用金属钠、钾的安全措施
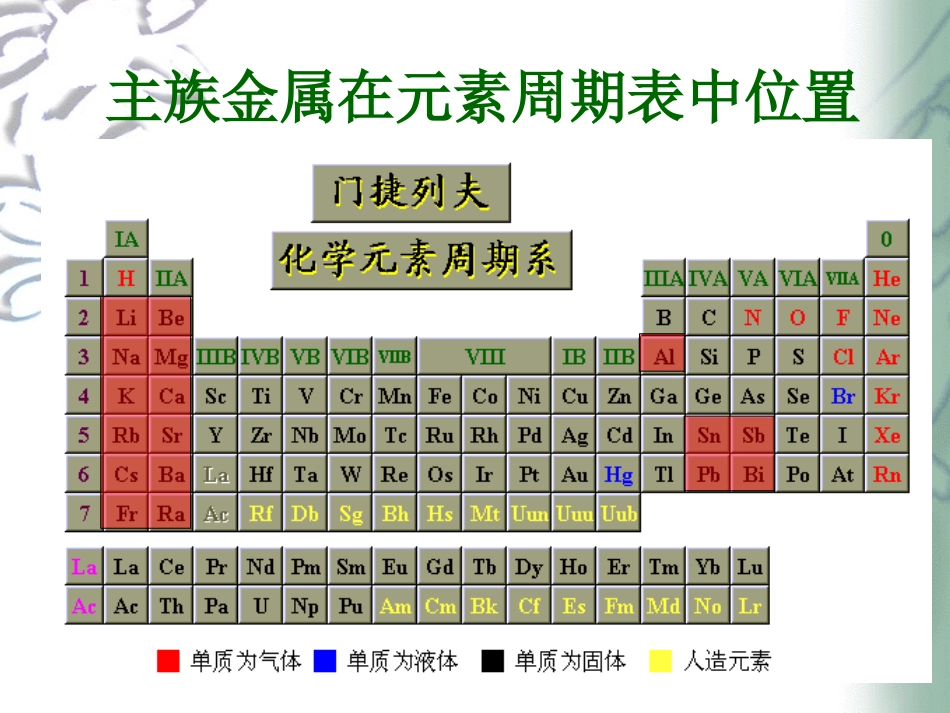
主族金属在元素周期表中位置主族金属元素性质氧化数+1+1+1+1+1氧化数+2+2+2+2+2ⅠALi(锂)Na(钠)K(钾)Rb(铷)Cs(铯)ⅡⅡABe(ABe(铍铍)Mg()Mg(镁镁)Ca()Ca(钙钙)Sr()Sr(锶锶)B)Ba(a(钡钡))电负性1
7E(M+/M)-3
026E(M2+/M)-1
912价电子构型ns1价电子构型ns2金属性递增金属性递增铝(Al)锡(Sn)铅(Pb)锑(Sb)铋(Bi)原子序数1350825183价层电子构型3s23p15s25p26s26p25s25p36s26p3主要氧化数0、+30、+2+40、+2+40、+3+50、+3+5原子半径/pm143141175141155E(Mn+/M)/V-1
308电负性()2
9p主族金属元素性质高氧化数化合物稳定性减小低氧化数化合物稳定性增大即惰性电子对效应明显惰性电子对效应明显φ/VA0
15Sn4+Sn2+Sn-0
454PbO2Pb2+Pb-0
126强氧化性实验内容•一、钠、钾、镁、铝的性质1
钠与空气中的氧气作用2
金属钠、钾、镁、铝与水作用注意:(1)铝与HgCl2反应生成了铝汞齐(2)注意使用金属钠、钾、汞的使用安全汞齐汞齐•又称汞合金,是汞与一种或几种其他金属所形成的合金,汞有一种独特的性质,它可以溶解多种金属(如金、银、钾、钠、锌等),